��Ŀ����
����Ŀ������50 kg�Ľ����˺�FeԪ��Լ2 g����Ҫ��Fe2����Fe3����ʽ�����������ڡ�Fe2���ױ����գ���ƶѪ�߲�������Ӧ���京Fe2����������(��FeSO4)������Vc����ʹʳ���е�Fe3��ת��ΪFe2����
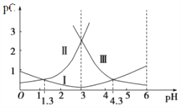
�������о�������Fe2��![]() Fe3����ת�����ڹ���A�У�Fe2����_______��������B��Fe3����______����
Fe3����ת�����ڹ���A�У�Fe2����_______��������B��Fe3����______����
��VcʹFe3��ת��ΪFe2����VC����һ��������___________������____________�ԡ�
���𰸡���ԭ�� ������ ��ԭ�� ��ԭ
��������
�ٹ���A��FeԪ�صĻ��ϼ�����������B��FeԪ�صĻ��ϼ۽�����
��VcʹFe3��ת��ΪFe2����FeԪ�صĻ��ϼ۽�������Vc����һ������ijԪ�صĻ��ϼ�������
�ٹ���A��FeԪ�صĻ��ϼ���������Fe2������ԭ��������B��FeԪ�صĻ��ϼ۽�������Fe3����������������ԭ��
��ˣ�������ȷ��������ԭ������������
��VcʹFe3��ת��ΪFe2����FeԪ�صĻ��ϼ۽�������Vc����һ������ijԪ�صĻ��ϼ�������������ԭ�������л�ԭ����
��ˣ�������ȷ��������ԭ������ԭ��

 Ӧ������ҵ��ϵ�д�
Ӧ������ҵ��ϵ�д�����Ŀ����������(POCl3)�������뵼����Ӽ������άԭ��,ʵ�����Ʊ�POCl3���ⶨ��Ʒ������ʵ��������£�
���Ʊ�POCl3��
������������Һ̬PCl3����ȡPOCl3,ʵ��װ��(���ȼ��г�������)��ͼ��ʾ��
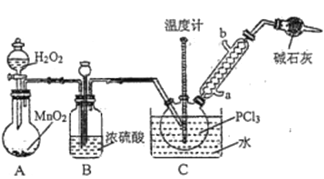
��֪����Ag++SCN-=AgSCN��;Ksp(AgCl)>Ksp(AgSCN);�������������ᡣ
��PCl3��POCl3�������Ϣ���±���
���� | �۵�/�� | �е�/�� | ��Է������� | ���� |
PCl3 | -112.0 | 76.0 | 137.5 | ������,��Ϊ��ɫҺ��,��ˮ�����ҷ�Ӧ���ɺ�������Ȼ��� |
POCl3 | 2.0 | 106.0 | 153.5 |
(1)POCl3��ˮ��Ӧ�Ļ�ѧ����ʽΪ_________________________________________��
(2)װ��B�����ó�����O2��,����_________________________________________������ܵ�������_______________��
(3)��Ӧ�¶�Ҫ������60~65��,ԭ����_____________________________________________��
�ⶨPOCl3��Ʒ�ĺ�����
ʵ�鲽�裺
���Ʊ�POCl3ʵ�������������ƿ�е�Һ����ȴ�����£�ȷ��ȡ30.7gPOCl3��Ʒ,����ʢ��60.00mL����ˮ��ˮ��ƿ��ҡ������ȫˮ��,��ˮ��Һ���100.00mL��Һ��
��ȡ10.00mL��Һ����ƿ��,����10.00mL3.2mol/LAgNO3����Һ��
�ۼ�����������������ҡ����ʹ�������汻�л��︲�ǡ�
����XΪָʾ��,��0.2mol/LKSCN��Һ�춨������AgNO3��Һ���ﵽ�ζ��յ�ʱ����ȥ10.00mLKSCN��Һ��
(4)������м�����������������___________________________________________�����˲���,�����Ʒ����Ԫ�ص�������������__________(�ƫ����ƫС�����䡱)��
(5)�������XΪ__________,��Ʒ��POCl3����������Ϊ____________��