题目内容
在250C、101kPa,1g甲醇燃烧生成二氧化碳和液态水放热22.7 kJ, 甲醇燃烧热的热化学方程式书写正确的是
A.CH3OH(l) + 3/2O2(g)= CO2(g) + 2H2O(l) △H= -726.4 kJ/mol
B.2CH3OH(l) + 3O2(g)= 2CO2(g) + 4H2O(l) △H=" -1452.8" kJ/mol
C.2CH3OH(l) + 3O2(g)= 2CO2(g) + 4H2O(l) △H= -726.4 kJ/mol
D.2CH3OH(l) + 3O2(g)= 2CO2(g) + 4H2O(l) △H= +1452.8 kJ/mol
A.CH3OH(l) + 3/2O2(g)= CO2(g) + 2H2O(l) △H= -726.4 kJ/mol
B.2CH3OH(l) + 3O2(g)= 2CO2(g) + 4H2O(l) △H=" -1452.8" kJ/mol
C.2CH3OH(l) + 3O2(g)= 2CO2(g) + 4H2O(l) △H= -726.4 kJ/mol
D.2CH3OH(l) + 3O2(g)= 2CO2(g) + 4H2O(l) △H= +1452.8 kJ/mol
A
试题分析:甲醇燃烧是放热反应,△H小于0,D不正确;1g甲醇燃烧生成二氧化碳和液态水放热22.7 kJ,所以1mol甲醇完全燃烧放出的热量是32×22.7kJ=726.4kJ,答案选A。
点评:该题是中等难度的试题,也是高考中的常见题型和考点。试题基础性强,难易适中,注重基础知识的巩固,侧重能力的培养。有助于培养学生的应试能力,提高学生学习效率。该题的关键是理解热化学方程式的含义以及书写时的注意事项即可。

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
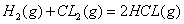 )在光照和点燃条件的△H相同
)在光照和点燃条件的△H相同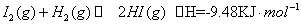
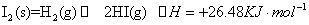
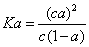 。若加入少量醋酸钠固体,则CH3COOH;—一CH3COO -十H+向左移动,a减小,Ka变小若加入少量醋酸钠固体,则
。若加入少量醋酸钠固体,则CH3COOH;—一CH3COO -十H+向左移动,a减小,Ka变小若加入少量醋酸钠固体,则
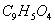 十H+向左移动,a减小,Ka变小
十H+向左移动,a减小,Ka变小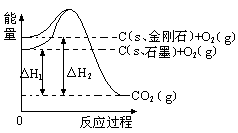
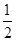 O2(g)△H= +242kJ·mol-1
O2(g)△H= +242kJ·mol-1