题目内容
【题目】如图表示反应N2(g)+3H2(g) ![]() 2NH3(g)+92.2kJ。在某段时间t0~t6中反应速率与反应过程的曲线图,则氨的百分含量最高的一段时间是( )
2NH3(g)+92.2kJ。在某段时间t0~t6中反应速率与反应过程的曲线图,则氨的百分含量最高的一段时间是( )
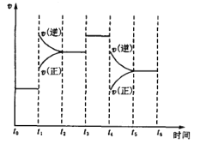
A.t0~t1B.t2~t3C.t3~t4D.t5~t6
【答案】A
【解析】
可逆反应N2(g)+3H2(g)2NH3(g)+92.2kJ,该反应为气体体积减小的放热反应,t0~t1,正、逆反应速率相等,为平衡状态;
t1~t2,正、逆反应速率都增大,且逆反应速率大于正反应速率,平衡向逆反应方向移动,导致氨气的含量降低,氨气含量较t0~t1低;
t2~t3,正、逆反应速率相等,处于平衡状态,氨气的含量不变,氨气含量较t1~t2低;
t3~t4,正、逆反应速率都同等程度的增大,平衡不移动,氨气的含量不变,氨气含量与t2~t3相同,氨气含量较t1~t2低;
t4~t5,正、逆反应速率都降低,但逆反应速率大于正反应速率,平衡向逆反应方向移动,氨气的含量降低,氨气含量较t2~t3低;
t5~t6,正、逆反应速率相等,平衡不移动,氨气的含量不变,氨气含量较t2~t3低;
所以平衡混合物中氨的百分含量最高的一段时间是t0~t1,故选A。

【题目】Ⅰ.某温度时,在一个10L的恒容容器中X、Y、Z均为气体,三种物质的物质的量随时间的变化曲线如图所示。根据图中数据填空:
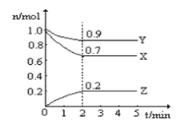
⑴该反应的化学方程式为___________;
⑵反应开始至2min,以气体Z表示的平均反应速率为___________;
⑶平衡时容器内混合气体密度比起始时_________(填“变大”,“变小”或“不变”下同),混合气体的平均相对分子质量比起始时___________;
⑷将amolX与bmolY的混合气体发生上述反应,反应到某时刻各物质的量恰好满足:n(X)=n(Y)=2n(Z),则原混合气体中a:b=__________。
Ⅱ.已知硫代硫酸钠溶液与稀硫酸反应的化学方程式为Na2S2O3+H2SO4= Na2SO4+ SO2↑+S↓+H2O,某学习小组探究一定条件下影响化学反应速率的因素,如下表所示:
⑸对比实验I、III可以得出的结论是______________,实验I、II探究的是___________的浓度越大,该反应速率越快,若实验III、IV也想得出同样结论,X=___________,Y= _________。
实验序号 | 温度 | Na2S2O3溶液 | 稀H2SO4 | H2O | ||
V/mL | c/(molL-1) | V/mL | c/(molL-1) | V/mL | ||
I | 25 | 5 | 0.1 | 10 | 0.1 | 5 |
II | 25 | 5 | 0.2 | 5 | 0.2 | 10 |
III | 35 | 5 | 0.1 | 10 | 0.1 | 5 |
IV | 35 | 5 | 0.2 | X | 0.2 | Y |