题目内容
【题目】某化学课外活动小组为了验证元素非金属性递变规律,设计了如图所示的两套实验方案进行实验探究:
方案一:

(1)根据方案一装置回答以下问题:
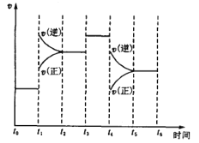
写出装置①发生的化学反应方程式:___。若将反应后②中的溶液倒入苯中,振荡静置后,出现的现象与如图吻合的是___。(填代号)装置③中的现象是___。

(2)根据方案二装置回答以下问题:
方案二:

方案二验证元素非金属性递变的理论依据是:___。B装置的作用是___,X试剂是___。
【答案】MnO2+4HCl(浓)![]() Cl2↑+MnCl2+2H2O C 溶液变蓝色 元素的非金属性越强,其最高价氧化物对应水化物的酸性越强 吸收CO2中的HCl 饱和NaHCO3溶液
Cl2↑+MnCl2+2H2O C 溶液变蓝色 元素的非金属性越强,其最高价氧化物对应水化物的酸性越强 吸收CO2中的HCl 饱和NaHCO3溶液
【解析】
(1)装置①中发生的是浓盐酸和二氧化锰反应生成氯化锰、氯气和水,若将反应后②中的溶液倒入苯中,溴单质和苯互溶,苯密度比水小,因此出现溶液分层,下层为无色,上层为橙红色,装置③中的现象是单质碘使淀粉溶液变蓝;
(2)方案二验证元素非金属性递变的理论依据是:元素的非金属性越强,最高价氧化物对应水化物的酸性越强。酸和盐反应生成新酸和新盐,则反应物的酸比生成物的酸的酸性强(以强酸制弱酸),A中生成二氧化碳,但含有易挥发的HCl,因此B装置的作用是除掉挥发出的HCl杂质,一般用饱和碳酸氢钠;据此分析解答。
(1)装置①中发生的是浓盐酸和二氧化锰反应,其化学方程式MnO2+4HCl(浓)![]() Cl2↑+MnCl2+2H2O,若将反应后②中的溶液倒入苯中,生成的溴单质和苯互溶,苯的密度比水小,因此出现溶液分层,下层为,上层为橙红色,则出现的现象与图中吻合的是C,生成的Cl2进入装置③中,将KI中的I-氧化成I2,使得淀粉溶液变蓝,故答案为:MnO2+4HCl(浓)
Cl2↑+MnCl2+2H2O,若将反应后②中的溶液倒入苯中,生成的溴单质和苯互溶,苯的密度比水小,因此出现溶液分层,下层为,上层为橙红色,则出现的现象与图中吻合的是C,生成的Cl2进入装置③中,将KI中的I-氧化成I2,使得淀粉溶液变蓝,故答案为:MnO2+4HCl(浓)![]() Cl2↑+MnCl2+2H2O;C;溶液变蓝色;
Cl2↑+MnCl2+2H2O;C;溶液变蓝色;
(2)方案二验证元素非金属性递变的理论依据是:元素的非金属性越强,最高价氧化物对应水化物的酸性越强,酸和盐反应生成新酸和新盐,则反应物的酸比生成物的酸的酸性强(以强酸制弱酸),A中生成二氧化碳,但含有易挥发的HCl,因此B装置的作用是除掉挥发出的HCl杂质,X是饱和碳酸氢钠,主要避免二氧化碳损失,故答案为:元素的非金属性越强,其最高价氧化物对应水化物的酸性越强;吸收CO2中的HCl;饱和NaHCO3溶液。