题目内容
(9分)硝基苯甲酸乙酯在OH-存在下发生水解反应:O2NC6H4COOC2H5+OH- O2NC6H4COO-+C2H5OH.两种反应物的初始浓度均为0.050mol/L,15 ℃时测得:O2NC6H4COOC2H5的转化率α随时间变化的数据如表所示。回答下列问题:
O2NC6H4COO-+C2H5OH.两种反应物的初始浓度均为0.050mol/L,15 ℃时测得:O2NC6H4COOC2H5的转化率α随时间变化的数据如表所示。回答下列问题:
| t/s | 0 | 120 | 180 | 240 | 330 | 30 | 600 | 700 | 800 |
| α/% | 0 | 33.0 | 41.8 | 48.8 | 58.0 | 69.0 | 70.4 | 71.0 | 71.0 |
(2)列式计算15 ℃时该反应的平衡常数_________________。
(3)为提高O2NC6H4COOC2H5的平衡转化率,除可适当控制反应温度外,还可以采取的措施有_________(要求写出两条)。
(1) ;
;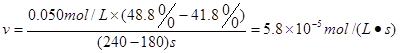 .随着反应的的进行,反应物的浓度降低,反应速率减慢 (2)
.随着反应的的进行,反应物的浓度降低,反应速率减慢 (2) 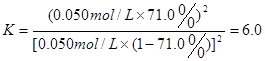 或
或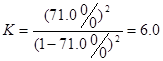 ; (3)增加OH-的浓度,移去产物。
; (3)增加OH-的浓度,移去产物。
解析试题分析:(1)根据题意结合表格的数据可知在120~180s内的反应速率是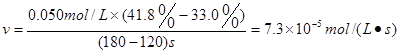 。在180~240s内的反应速率是
。在180~240s内的反应速率是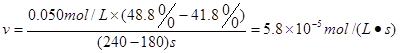 由反应速率的数值可以看出:随着反应的的进行,反应物的浓度降低,反应速率减慢。(2)在15 ℃时该反应的平衡常数是
由反应速率的数值可以看出:随着反应的的进行,反应物的浓度降低,反应速率减慢。(2)在15 ℃时该反应的平衡常数是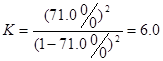 ;(3)为提高O2NC6H4COOC2H5的平衡转化率,除可适当控制反应温度外,还可以采取的措施有增加其它反应物浓度的方法或减小生成物浓度的方法。因此对该反应来说,就是可采取增大OH-的浓度,移去产物的方法。
;(3)为提高O2NC6H4COOC2H5的平衡转化率,除可适当控制反应温度外,还可以采取的措施有增加其它反应物浓度的方法或减小生成物浓度的方法。因此对该反应来说,就是可采取增大OH-的浓度,移去产物的方法。
考点:考查化学反应速率的计算、影响化学平衡移动的因素、化学平衡常数的表达式等知识。

 手拉手全优练考卷系列答案
手拉手全优练考卷系列答案利用“化学蒸气转移法”制备TaS2晶体,某温度下的2L恒容密闭容器中加入一定量 的 I2(g)和TaS2(s)发生如下反应
TaS2(s)+2I2(g) TaI4(g)+S2(g)△H=a kJ·mol-1 (I)
TaI4(g)+S2(g)△H=a kJ·mol-1 (I)
达平衡时,TaS2(s)、I2(g)、TaI4(g)、、S2(g)的物质的量分别为3 mol 、2mol、2mol、2mol。
(1)反应(I)的平衡常数表达式K=
(2)若该温度下该容器中某时刻TaS2(s)、I2(g)、TaI4(g)、、S2(g)的物质的量分别为2mol、2mol、4mol、4mol,则该时刻平衡向 (填“正反应”或“逆反应”)移动,v正 v逆(填“>”、“=”或“<”)。
(3)在不同温度下,该反应的平衡常数K如下表:
| 温度/℃ | 40 | 80 | 200 |
| 平衡常数K | 1 | 1.5 | 4 |
(4)40℃时,向该恒容密闭容器中加入2mol I2(g)和4mol TaS2(s),I2(g)的平衡转化率为 (写出计算过程,结果保留小数点后1位)
(12分).
在1.0 L密闭容器中放入0.10molA(g),在一定温度进行如下反应:
A(g) B(g)+C(g) △H=+85.1kJ·mol-1(吸热反应)
B(g)+C(g) △H=+85.1kJ·mol-1(吸热反应)
反应时间(t)与容器内气体总压强(p)的数据见下表:
| 时间t/h | 0 | 1 | 2 | 4 | 8 | 16 | 20 | 25 | 30 |
| 总压强p/100kPa | 4.91 | 5.58 | 6.32 | 7.31 | 8.54 | 9.50 | 9.52 | 9.53 | 9.53 |
回答下列问题:
(1)欲提高A的平衡转化率,应采取的措施为_______________。
(2)由总压强P和起始压强P0计算反应物A的转化率α(A)的表达式为_______。平衡时A 的转化率为_____.
(3) ①由总压强p和起始压强p0表示反应体系的总物质的量n总和反应物A的物质的量n(A),
n总=_______mol,n(A)=_______mol。
②下表为反应物A浓度与反应时间的数据,计算a= _______________
| 反应时间t/h | 0 | 4 | 8 | 16 |
| C(A)/(mol·L-1) | 0.10 | a | 0.026 | 0.0065 |
分析该反应中反应物的浓度c(A)变化与时间间隔(△t)的规律,得出的结论是_________________,由此规律推出反应在12h时反应物的浓度c(A)为_______mol·L-1
(15分)太阳能电池是利用光电效应实现能量变化的一种新型装置,目前多采用单晶硅和多晶硅作为基础材料。高纯度的晶体硅可通过以下反应获得:
反应①(合成炉):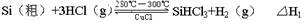
反应②(还原炉):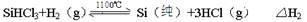
有关物质的沸点如下表所示:
| 物质 | BCl3 | PCl3 | SiCl4 | AsCl3 | AlCl3 | SiHCl3 |
| 沸点 | 12.1 | 73.5 | 57.0 | 129.4 | 180(升华) | 31.2 |
(1)太阳能电池的能量转化方式为 ;由合成炉中得到的SiHCl3往往混有硼、磷、砷、铝等氯化物杂质,分离出SiHCl3的方法是 。
(2)对于气相反应,用某组分(B)的平衡压强(PB)代替物质的量浓度(cB)也可表示平衡常数(记作KP),则反应①的KP= ;
(3)对于反应②,在0.1Mpa下,不同温度和氢气配比(H2/SiHCl3)对SiHCl3剩余量的影响如下表所示:
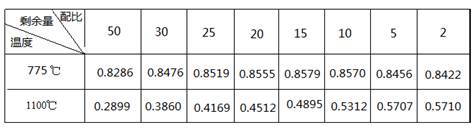
①该反应的△H2 0(填“>”、“<”、“=”)
②按氢气配比5:1投入还原炉中,反应至4min时测得HCl的浓度为0.12mol·L—1,则SiHCl3在这段时间内的反应速率为 。
③对上表的数据进行分析,在温度、配比对剩余量的影响中,还原炉中的反应温度选择在1100℃,而不选择775℃,其中的一个原因是在相同配比下,温度对SiHCl3 剩余量的影响,请分析另一原因是 。
(4)对于反应②,在1100℃下,不同压强和氢气配比(H2/SiHCl3)对SiHCl3剩余量的影响如图27—1所示:
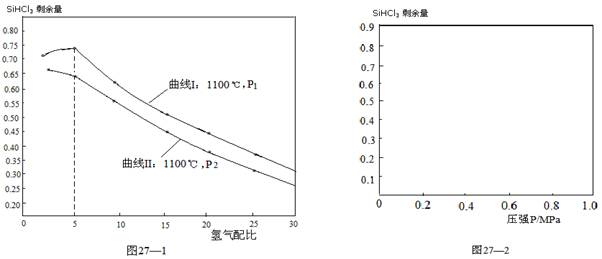
① 图中P1 P2(填“>”、“<”、“=”)
②在图27—2中画出氢气配比相同情况下,1200℃和1100℃的温度下,系统中SiHCl3剩余量随压强变化的两条变化趋势示意图。
(14分)短周期主族元素A、B、C、D、E原子序数依次增大 , A是元素周期表中原子半径最小的元素,B是形成化合物种类最多的元素,C原子的最外层电子数是次外层电子数的3倍,D是同周期中金属性最强的元素,E的负一价离子与C的某种氢化物分子含有相同的电子数。
⑴A、C、D形成的化合物中含有的化学键类型为 。
⑵已知:
① E-E→2E ?H=+a kJ/mol;
② 2A→A-A ?H=-b kJ/mol;
③ E+A→A-E ?H=-c kJ/mol;
写出298K时,A2与E2反应的热化学方程式 。
⑶在某温度下容积均为2 L的三个密闭容器中,按不同方式投入反应物,保持恒温恒容,使之发生反应:2A2(g)+BC(g) X(g) ?H=-Q kJ/mol(Q>0,X为A、B、C三种元素组成的一种化合物)。初始投料与各容器达到平衡时的有关数据如下:
X(g) ?H=-Q kJ/mol(Q>0,X为A、B、C三种元素组成的一种化合物)。初始投料与各容器达到平衡时的有关数据如下:
| 实验 | 甲 | 乙 | 丙 |
| 初始投料 | 2 mol A2、1 mol BC | 1 mol X | 4 mol A2、2 mol BC |
| 平衡时n(X) | 0.5 mol | n2 | n3 |
| 反应的能量变化 | 放出Q1kJ | 吸收Q2kJ | 放出Q3kJ |
| 体系的压强 | P1 | P2 | P3 |
| 反应物的转化率 |  1 1 |  2 2 |  3 3 |
v (A2)= 。
② 计算该温度下此反应的平衡常数K = 。
③三个容器中的反应分别达平衡时下列各组数据关系正确的是 (填字母)。
A.α1+α2=1 B.Q1+Q2=Q C.α3<α1
D.P3<2P1=2P2 E.n2<n3<1.0 mol F.Q3=2Q1
④在其他条件不变的情况下,将甲容器的体积压缩到1 L,若在第8min达到新的平衡时A2的总转化率为75%,请在下图中画出第5min 到新平衡时X的物质的量浓度的变化曲线。
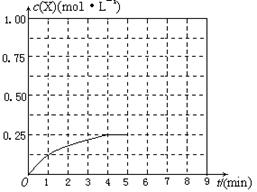
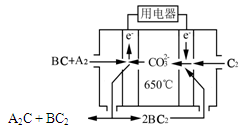
⑷熔融碳酸盐燃料电池(MCFC)是一种高温燃料电池,被称为第二代燃料电池,是未来民用发电的理想选择方案之一,其工作原理如图所示。现以A2(g)、BC(g)为燃料,以一定比例Li2CO3和Na2CO3低熔混合物为电解质。写出该碳酸盐燃料电池(MCFC)正极的电极反应式____________________________。
温度为T时,向2.0 L恒容密闭容器中充入1.0 mol PCl5,反应PCl5(g) PCl3(g)+Cl2(g)经过一段时间后达到平衡。反应过程中测定的部分数据如图:
PCl3(g)+Cl2(g)经过一段时间后达到平衡。反应过程中测定的部分数据如图:
下列说法正确的是
| A.反应在前50 s 的平均速率v(PCl3)=0.0032 mol·L-1·s-1 |
| B.保持其他条件不变,升高温度,平衡时c(PCl3)=0.11mol·L-1,则反应的△H<0 |
| C.相同温度下,起始时向容器中充入2.0 mol PCl3和2.0mol Cl2,达到平衡时,PCl3的转化率小于80% |
| D.相同温度下,起始时向容器中充入1.0 mol PCl5、0.20mol PCl3和0.20 mol Cl2,反应达到平衡前v(正)>v(逆) |



 ,得到如下两组数据:
,得到如下两组数据:
 ____________
____________ (填“<”,“>”,“=”)。
(填“<”,“>”,“=”)。

 。CaCl2溶液与Na2CO3溶液混合可形成CaCO3沉淀,现将等体积的CaCl2溶液与Na2CO3溶液混合,若Na2CO3溶液的浓度为1×10
。CaCl2溶液与Na2CO3溶液混合可形成CaCO3沉淀,现将等体积的CaCl2溶液与Na2CO3溶液混合,若Na2CO3溶液的浓度为1×10 mol/L,则生成沉淀所需CaCl2溶液的最小浓度为__________mol/L。
mol/L,则生成沉淀所需CaCl2溶液的最小浓度为__________mol/L。 Ni(CO)4(g)
Ni(CO)4(g)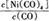 减小,则?H 0(填“>”或“<”)。
减小,则?H 0(填“>”或“<”)。
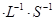 。
。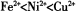 )
)