题目内容
用图中所示实验装置证明氧化铜能加快约7%的双氧水的分解并与二氧化锰的催化效果进行比较(即比较反应速率)。用图示装置测量产生气体的体积,其他可能影响实验的因素均已忽略,相关数据如下:
(1)从实验原理来看,实验中的“待测数据”可以指、也可以指 。
(2)实验时气体收集在B中,B仪器名称是__________。若要检验产生的气体是O2,待气体收集结束 后,用弹簧夹夹住B下端乳胶管,打开单孔橡皮塞, 。
(3)为探究CuO在实验②中是否起催化作用,除与①比较外,还需补做下列实验不必写具体步骤):a.证明CuO的化学性质没有变化,b. 。
(4)为证明氧化铜的化学性质在加入双氧水前后没有发生改变,你设计验证的实验是 。
(5)实验开始时,当往容器中加入一定量的双氧水后,由于短时间内产生大量气体,分液漏斗内的液体不能顺利流下,为了解决这个问题,你采取的措施是 ;在测量生成的气体体积时,除了要注意视线与凹液面相平以外,还应注意
(1)时间和气体体积或相同时间内放出气体所占的体积(或一定时间内右侧水面上升的高度);也可以指产生相同体积气体所需要的时间
(2)干燥管;把带火星的木条插入干燥管,看是否复燃
(3)证明CuO的质量在反应前后没有变化
(4)分别取加入双氧水前后的氧化铜,进行与H2(或CO、C等还原剂)的反应或与酸溶液的反应的性质实验比较
(5)使塞子上的凹槽对准瓶壁上小孔;左右两端液面相平;反应前后容器温度相同
解析试题分析:(1)根据题意知,该实验的目的是比较反应速率,所以实验中的“待测数据”可以指时间和气体体积或相同时间内放出气体所占的体积(或一定时间内右侧水面上升的高度);也可以指产生相同体积气体所需要的时间。(2)根据仪器的构造特点可知,B仪器名称是干燥管。氧气是助燃性气体,所以检验氧气的实验方法是把带火星的木条插入干燥管,看是否复燃。(3)判断一种物质是催化剂,除能改变反应速度外,还要验证:一是质量不变,二是其化学性质不变,即证明CuO的质量在反应前后没有变化。(4)根据氧化铜的化学性质可知,要证明氧化铜的化学性质在加入双氧水前后没有发生改变,设计验证的实验可以是分别取加入双氧水前后的氧化铜,进行与H2(或CO、C等还原剂)的反应或与酸溶液的反应的性质实验比较。(5)要使液体顺利滴下则应该是内外压强相同,所以采取的措施是使塞子上的凹槽对准瓶壁上小孔;在测量气体体积时,应该是两侧的压强相同,且温度也是相同,所以措施是使左右两端液面相平,且反应前后容器温度相同。
考点:考查反应速率测定实验的探究、仪器的识别、氧气的检验、催化剂的验证以及基本实验操作。

一定温度下,可逆反应H2(g)+I2(g) 2HI(g)达到化学平衡状态的标志是( )
2HI(g)达到化学平衡状态的标志是( )
| A.混合气体的压强不再变化 | B.混合气体的颜色不再变化 |
| C.反应速率v(H2)="0.5v" (HI) | D.c (H2):c(I2):c(HI)=1:1:2 |
(7分)CO可用于合成甲醇,一定温度下,向体积为2L的密闭容器中加入CO和H2,发生反应CO(g)+2H2(g) CH3OH(g),达平衡后测得各组分浓度如下:
CH3OH(g),达平衡后测得各组分浓度如下:
| 物质 | CO | H2 | CH3OH |
| 浓度(mol?L-1) | 0.9 | 1.0 | 0.6 |
②列式并计算平衡常数K=__________________________。
③若将容器体积压缩为1L,不经计算,预测新平衡中c(H2)的取值范围是__________。
④若保持体积不变,再充入0.6molCO和0.4molCH3OH,此时v正___v逆(填“>”、“<”或“=”)。
(9分)硝基苯甲酸乙酯在OH-存在下发生水解反应:O2NC6H4COOC2H5+OH- O2NC6H4COO-+C2H5OH.两种反应物的初始浓度均为0.050mol/L,15 ℃时测得:O2NC6H4COOC2H5的转化率α随时间变化的数据如表所示。回答下列问题:
O2NC6H4COO-+C2H5OH.两种反应物的初始浓度均为0.050mol/L,15 ℃时测得:O2NC6H4COOC2H5的转化率α随时间变化的数据如表所示。回答下列问题:
| t/s | 0 | 120 | 180 | 240 | 330 | 30 | 600 | 700 | 800 |
| α/% | 0 | 33.0 | 41.8 | 48.8 | 58.0 | 69.0 | 70.4 | 71.0 | 71.0 |
(2)列式计算15 ℃时该反应的平衡常数_________________。
(3)为提高O2NC6H4COOC2H5的平衡转化率,除可适当控制反应温度外,还可以采取的措施有_________(要求写出两条)。
 CO2(g) + H2(g) △H < 0,下列措施能提高反应速率的有 (不定项选择)。
CO2(g) + H2(g) △H < 0,下列措施能提高反应速率的有 (不定项选择)。 2SO3 测得平衡时混合物总物质的量为5mol,求:
2SO3 测得平衡时混合物总物质的量为5mol,求: N2O4(g) (无色),如图所示。
N2O4(g) (无色),如图所示。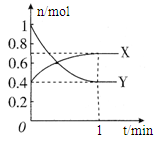
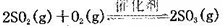 (正反应放热)。测得n(O2)随时间的变化如下表
(正反应放热)。测得n(O2)随时间的变化如下表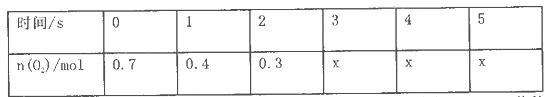
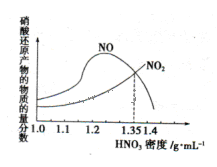
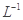 的硝酸反应的化学方程式:______________________.
的硝酸反应的化学方程式:______________________.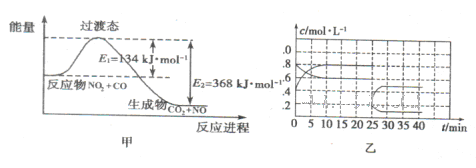
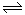 N2O4(g) △H<0。现将一定量的NO2和N2O4混合气体通入体积为1L的恒温密闭容器中发生上述反应,反应物的浓度随时问变化关系如图乙所示。
N2O4(g) △H<0。现将一定量的NO2和N2O4混合气体通入体积为1L的恒温密闭容器中发生上述反应,反应物的浓度随时问变化关系如图乙所示。