题目内容
【题目】实验室中用如图所示的原电池装置做电源电解足量的NaC1的酚酞溶液,X、Y均为惰性电极。下列有关说法不正确的是
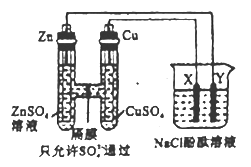
A. 原电池中SO42-通过隔膜从左向右移动
B. 反应一段时间后,烧杯中Y电极附近变红
C. Zn极质量减少6.5g时,X极理论上生成气体2.24L(标准状况)
D. 室温下,若Cu极质量增加1.6g时,此时烧杯溶液体积为500mL,则溶液的pH为13
【答案】A
【解析】左边原电池中锌比较活泼做为负极,铜做为正极,X连接正极则为阳极,Y连接负极则为阴极。A、原电池中阴离子向负极移动,则应从右向左移动,选项A不正确;B、Y电极是阴极,溶液中的氢离子在Y极得电子产生氢气,则氢氧根离子浓度增大,遇酚酞变红,选项B正确;C、Zn极质量减少6.5g时,转移电子数为0.2mol,X极氯离子得电子产生氯气,转移0.2mol电子时理论上生成气体2.24L(标准状况),选项C正确;D、室温下,若Cu极质量增加1.6g时,即析出0.025mol铜,转移电子数为0.05mol,此时烧杯溶液中有0.05mol氢离子得电子产生氢气,则增加的氢氧根离子0.05mol,溶液体积为500mL,则溶液中c(OH-)=![]() =0.1mol/L,c(H+)=10-13mol/L,溶液pH为13,选项D正确。答案选A。
=0.1mol/L,c(H+)=10-13mol/L,溶液pH为13,选项D正确。答案选A。

练习册系列答案
 小学能力测试卷系列答案
小学能力测试卷系列答案
相关题目
【题目】下列有关有机物同分异构体数目的叙述中,正确的是
选项 | 有机物 | 同分异构体数目 |
A | 二氯甲烷 | 2种 |
B | C8H10中属于芳香烃的有机物 | 3种 |
C | 分子式为C5H11Br的卤代烃 | 8种 |
D | 分子式为C7H8O且属于芳香族有机物 | 5种 |
A. A B. B C. C D. D





