题目内容
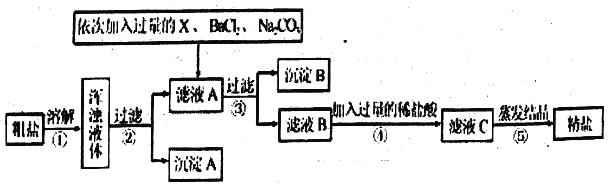
【题目】海水晒盐可制得粗盐,粗盐除氯化钠外,还含有MgCl2、CaCl2、Na2SO4以及泥沙等杂质,以下是某化学兴趣小组制定的一套制备精盐的实验方案,步骤如图所示:
【査阅资料】可溶性钡盐有剧毒,可以导致蛋白质变性,破坏体内各种酶,使一系列生理活动被破坏。
【交流与表达】
(1)步驟①中玻璃棒的作用是________,溶解粗盐时所加水的质量不宜过多,也不宜过少,过多则蒸发时浪费燃料并且耗时长,过少会使得精盐的产率________(填"偏高"或“偏低”);
(2)下列试剂X符合要求的是_______ (选填字母)。
A、氧化钙 B、氢氧化钡溶液 C、氢氧化钠溶液 D、氢氧化钙溶液 E、氢氧化钾溶液
(3)氯化钡溶液和碳酸钠溶液的添加顺序_______(填“能”或“不能”)颠倒,沉淀B中的成分是BaSO4和_______(填化学式)。
(4)进行操作③后,下列判断Na2CO3过量的方法正确的是_______ (选填字母)。
A、 取少量滤液B,滴加酚酞,若变为红色,说明Na2CO3过量
B、 取少量滤液B,滴加足量稀盐酸,若有气泡产生,说明Na2CO3过量
C、 取少量滤液B,滴加氣化钡溶液,若有白色沉淀产生,说明Na2CO3过量
(5)某同学为了证明溶液C是否有盐酸剩余,设计的下列方法中正确的是_______(选填宇母)。
A、 取样,加入铜,若无现象,说明盐酸没有剩余
B、 取样,测溶液pH,若PH<7,说明盐酸有剩余
C、 取样,加碳酸钠溶液,若有气泡产生,说明有盐酸剩余
D、 取样,滴入酚酞溶液,若溶液呈无色,说明盐酸有剩余
E、 取样,加硝酸银溶液,若有白色沉淀产生,说明有盐酸剩余
【反思与评价】(6)小刚同学认为该方案实际得到的氯化钠比原粗盐中含有的氯化钠要多, 请你为他找出理由_______________。
【答案】 加快溶解速率 偏低 ABCD 不能 CaCO3 、BaCO3、Mg(OH)2 BC BC 在提纯过程中反应生成了氯化钠
【解析】(1)步骤①中玻璃棒的作用是加快溶解速率;溶解粗盐时所加水的质量不宜过多,也不宜过少,过多时,蒸发时浪费燃料并且耗时长,也不宜过少,过少时会导致氯化钠不能完全溶解,导致精盐的产率偏低;(2)A、氧化钙和水反应生成氢氧化钙,氢氧化钙能和氯化镁反应生成氢氧化镁沉淀和氯化钙,因此X可以是氧化钙,A正确; B、氢氧化钡和氯化镁反应生成氢氧化镁沉淀和氯化钡,因此X可以是氢氧化钡溶液,B正确; C、氢氧化钠和氯化镁反应生成氢氧化镁沉淀和氯化钠,因此X可以是氢氧化钠溶液,C正确; D、氢氧化钙能和氯化镁反应生成氢氧化镁沉淀和氯化钙,因此X可以是氢氧化钙溶液,D正确; E、氢氧化钾和氢氧化镁反应生成氢氧化镁沉淀和氯化钾,和稀盐酸反应生成氯化钾和水,X是氢氧化钾溶液时会带入杂质氯化钾,因此X不能是氢氧化钾溶液,E错误,答案选ABCD;(3)氯化钡溶液和碳酸钠溶液的添加顺序不能颠倒,这是因为颠倒后不能除去过量的氯化钡;根据以上分析可知沉淀B中的成分是BaSO4、CaCO3和BaCO3、Mg(OH)2。(4)A、取少量滤液B,滴加酚酞,若变为红色,不能说明Na2CO3过量,这是因为溶液中含有氢氧化钠,氢氧化钠溶液能使酚酞试液变红色,A错误;B、取少量滤液B,滴加足量稀盐酸,若有气泡产生,说明Na2CO3过量;C、取少量滤液B,滴加氯化钡溶液,若有白色沉淀产生,说明Na2CO3过量,答案选BC;(5)A、取样,加入铜,若无现象,不能说明盐酸没有剩余,这是因为铜不能和稀盐酸反应,A错误;B、取样,测溶液pH,若pH<7,说明盐酸有剩余,B正确;C、取样,加碳酸钠溶液,若有气泡产生,说明有盐酸剩余,C正确;D、取样,滴入酚酞溶液,若溶液呈无色,不能说明盐酸没有剩余,这是因为盐酸显酸性,不能使酚酞试液变色,D错误;E、取样,加硝酸银溶液,若有白色沉淀产生,不能说明有盐酸剩余,这是因为氯化钠能和硝酸银反应生成白色沉淀氯化银,E错误,答案选BC;(6)该方案实际得到的氯化钠比原粗盐中含有的氯化钠要多,折是因为反应中生成了氯化钠。

 阅读快车系列答案
阅读快车系列答案