��Ŀ����
5��M��KΪ��ҵ�����г��õ����ָ߾����ϳ�·�����£�����J�������Ȼ�����Һ�ܷ�����ɫ��Ӧ���ұ����ϵ�һԪȡ���������֣�
��֪��
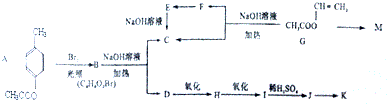
�ٵ��ǻ���˫��̼ԭ������ʱ����������ת��RCH=CHOH��RCH2CHO
��-ONa���������ϲ��ᱻ����
��ش��������⣺
��1��д��M�Ľṹ��ʽ
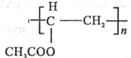 ��B�о��еĹ����ŵ�������������ԭ�ӣ�
��B�о��еĹ����ŵ�������������ԭ�ӣ���2�������仯��G��C+F�ķ�Ӧ������ˮ�ⷴӦ��ȡ����Ӧ��J��һ�������������ɸ߾���K��K�Ľṹ��ʽ��
 ��
����3��д��B��C+D��Ӧ�Ļ�ѧ����ʽ��
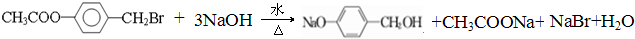 ��
����4��ͬʱ��������Ҫ���A��ͬ���칹����14�֣�
�����
���ܷ���������Ӧ��ˮ�ⷴӦ
��д����������������ͬ���칹��ṹ��ʽ��
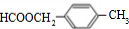 ��
���ٺ˴Ź���������5�����շ�
��1mol��ͬ���칹������1molNaOH��Ӧ
��5�������й�˵������ȷ����ad��
a.1molA��ȫȼ�����ı�״����246.4LO2
b.1molJ��������̼��������Һ��Ӧ������1mol̼������
c��D��I���Լ�ͨ����������KMnO4��Һ
d��J�ܷ����ӳɡ���ȥ��ȡ���������ȷ�Ӧ��
���� MΪCH3COOCH=CH2���ɵĸ߷��ӻ������MΪ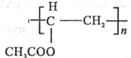 ��G����������ˮ�ܡ�������������������C��F��F����ת���õ�C����FΪCH3CHO��EΪCH3COOH��CΪCH3COONa��B����������ˮ��Һ����������������C��D��D����������������I����B����������I�ữ�õ���J���Ȼ�����Һ������ɫ��Ӧ��˵��J�к��з��ǻ�����B���б�������J�л��ϵ�һԪȡ����ֻ�����ֽṹ��Ӧ����2����ͬ�����Ҵ��ڶ�λ�����Ϸ�����֪BΪ
��G����������ˮ�ܡ�������������������C��F��F����ת���õ�C����FΪCH3CHO��EΪCH3COOH��CΪCH3COONa��B����������ˮ��Һ����������������C��D��D����������������I����B����������I�ữ�õ���J���Ȼ�����Һ������ɫ��Ӧ��˵��J�к��з��ǻ�����B���б�������J�л��ϵ�һԪȡ����ֻ�����ֽṹ��Ӧ����2����ͬ�����Ҵ��ڶ�λ�����Ϸ�����֪BΪ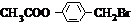 ����DΪ
����DΪ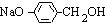 ��HΪ
��HΪ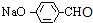 ��I�Ľṹ��ʽΪ��
��I�Ľṹ��ʽΪ��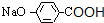 ��
�� ��JΪ
��JΪ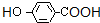 ���߾���KΪ
���߾���KΪ ���ݴ˽��н��
���ݴ˽��н��
��� �⣺MΪCH3COOCH=CH2���ɵĸ߷��ӻ������MΪ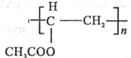 ��G����������ˮ�ܡ�������������������C��F��F����ת���õ�C����FΪCH3CHO��EΪCH3COOH��CΪCH3COONa��B����������ˮ��Һ����������������C��D��D����������������I����B����������I�ữ�õ���J���Ȼ�����Һ������ɫ��Ӧ��˵��J�к��з��ǻ�����B���б�������J�л��ϵ�һԪȡ����ֻ�����ֽṹ��Ӧ����2����ͬ�����Ҵ��ڶ�λ�����Ϸ�����֪BΪ
��G����������ˮ�ܡ�������������������C��F��F����ת���õ�C����FΪCH3CHO��EΪCH3COOH��CΪCH3COONa��B����������ˮ��Һ����������������C��D��D����������������I����B����������I�ữ�õ���J���Ȼ�����Һ������ɫ��Ӧ��˵��J�к��з��ǻ�����B���б�������J�л��ϵ�һԪȡ����ֻ�����ֽṹ��Ӧ����2����ͬ�����Ҵ��ڶ�λ�����Ϸ�����֪BΪ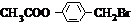 ����DΪ
����DΪ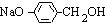 ��HΪ
��HΪ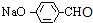 ��I�Ľṹ��ʽΪ��
��I�Ľṹ��ʽΪ��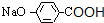 ��
�� ��JΪ
��JΪ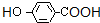 ���߾���KΪ
���߾���KΪ ��
��
��1��������������֪��M�Ľṹ��ʽΪ��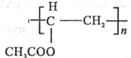 ��B�Ľṹ��ʽΪ��
��B�Ľṹ��ʽΪ��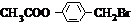 �����еĹ�����Ϊ��������ԭ�ӣ�
�����еĹ�����Ϊ��������ԭ�ӣ�
�ʴ�Ϊ��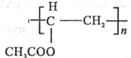 ����������ԭ�ӣ�
����������ԭ�ӣ�
��2�������仯��G��C+F��������ˮ�ⷴӦ��Ҳ����ȡ����Ӧ��JΪ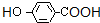 ����һ�������·������۷�Ӧ���ɸ߾���KΪ
����һ�������·������۷�Ӧ���ɸ߾���KΪ ��
��
�ʴ�Ϊ��ˮ�ⷴӦ��ȡ����Ӧ�� ��
��
��3��B��C+D��Ӧ�Ļ�ѧ����ʽ��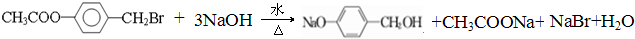 ��
��
�ʴ�Ϊ��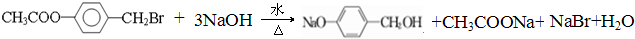 ��
��
��4��ͬʱ��������Ҫ���A�� ����ͬ���칹�壺���б��������ܷ���������Ӧ��ˮ�ⷴӦ��Ӧ�Ǽ�������ֻ��һ������Ϊ-CH2CH2OOCH��-CH��CH3��OOCH��������������-CH2CH3��-OOCH������-CH3��-CH2OOCH�������ڡ��䡢�����֣�������������Ϊ2��-CH3��1��-OOCH��2��-CH3���ڡ��䡢�����֣���Ӧ-OOCH��2�֡�3�֡�1�֣��ʷ���������A��ͬ���칹���У�2+6+2+3+1=14�֣�
����ͬ���칹�壺���б��������ܷ���������Ӧ��ˮ�ⷴӦ��Ӧ�Ǽ�������ֻ��һ������Ϊ-CH2CH2OOCH��-CH��CH3��OOCH��������������-CH2CH3��-OOCH������-CH3��-CH2OOCH�������ڡ��䡢�����֣�������������Ϊ2��-CH3��1��-OOCH��2��-CH3���ڡ��䡢�����֣���Ӧ-OOCH��2�֡�3�֡�1�֣��ʷ���������A��ͬ���칹���У�2+6+2+3+1=14�֣�
���������������ٺ˴Ź���������5 �����շ壻��1mol��ͬ���칹������1mol NaOH ��Ӧ��Ӧ�Ǽ����봼�γɵ������ʷ��������� ��ͬ���칹��Ϊ��
��ͬ���칹��Ϊ��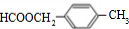 ��
��
�ʴ�Ϊ��14��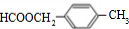 ��
��
��5��a��A�ķ���ʽΪC9H10O2��1mol A ��ȫȼ������ O2Ϊ��9+$\frac{10}{4}$-$\frac{2}{2}$��mol=10.5mol�������10.5mol���������Ϊ��22.4L/mol��10.5mol=235.2L����a����
b�� JΪ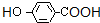 �����ǻ�����̼�����Ʒ�Ӧ���Ȼ���̼�����Ʒ�Ӧ��1molJ�ܹ�����1mol̼�����ƣ���b��ȷ��
�����ǻ�����̼�����Ʒ�Ӧ���Ȼ���̼�����Ʒ�Ӧ��1molJ�ܹ�����1mol̼�����ƣ���b��ȷ��
c�� D��I��Ҫ����ǿ��������ͨ�������Ը��������Һ����c��ȷ��
d�� 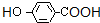 ���б������������������ӳɷ�Ӧ�����з��ǻ����Ȼ����ܷ���ȡ����Ӧ�����ǻ��ܷ���������Ӧ���ҿ���ȼ�գ�Ҳ����������Ӧ�����ܷ�����ȥ��Ӧ����d����
���б������������������ӳɷ�Ӧ�����з��ǻ����Ȼ����ܷ���ȡ����Ӧ�����ǻ��ܷ���������Ӧ���ҿ���ȼ�գ�Ҳ����������Ӧ�����ܷ�����ȥ��Ӧ����d����
��ѡ��ad��
���� ���⿼���л�����ƶϣ���Ŀ�ѶȽϴ�Ϊ�߿��ȵ㣬�Ƕ��л���֪ʶ���ۺ����ã�����G�ļӾ۲���Ľṹ��ʽ�ж�G�Ľṹ��ʽ���ƶϵĹؼ������������Ʒ������Ʒ�����ƶ��������ʣ�ע�������÷�Ӧ��������5����ͬ���칹����Ŀ�ж�����������ͬ���칹����дΪ�״��㡢�ѵ㣬��Ҫѧ���Ը������Ϣ�������ã��ܽϺõĿ��鿼�����Ķ�����ѧ������˼ά������

 ��ս�п�����ϵ�д�
��ս�п�����ϵ�д�| A�� | 0.1mol/LCH3COONa��Һ��0.1mol/L HCl��Һ�������ϣ�c��Na+����c��Cl-����c��CH3COO-����c��OH-�� | |
| B�� | 0.1mol/L NH4Cl��Һ��0.1mol/L��ˮ�������ϣ�pH��7����c��NH3��H2O����c��NH4+����c��Cl-����c��OH-�� | |
| C�� | 0.1mol/L Na2CO3��0.1mol/LNaHCO3��Һ�������ϣ�2c��Na+��=3c��HCO3-��+3c��CO32-��+3c��H2CO3�� | |
| D�� | 0.1mol/LCH3COOH��Һ��0.1mol/LNaOH��Һ�������ϣ�������Һ�У�c��OH-����c��H+��+c��CH3COOH�� |
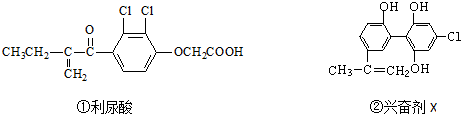
��������ǵ�˵������ȷ���ǣ�������
| A�� | ����������������ֺ��������ţ��ں˴Ź��������Ϲ��������� | |
| B�� | 1 mol�˷ܼ�X������Ũ��ˮ��Ӧ���������4 mol Br2 | |
| C�� | �����˷ܼ����ܺͺ�3molNaOH����Һ��Ӧ | |
| D�� | ���ַ����е�����̼ԭ�Ӿ������ܹ�ƽ�� |
��1��PM2.5������������Ļ�������ж��°����ʣ����Ԫ�ط���ΪAs��λ��Ԫ�����ڱ��������ڵڢ�A�壮
��2����PM2.5����������ˮ�����ɴ���Һ���������ˮ���������ӵĻ�ѧ��ּ���ƽ��Ũ�����±���
| ���� | K+ | Na+ | NH4+ | SO42- | NO3- | Cl- |
| Ũ��/mol•L-1 | 4��10-6 | 6��10-6 | 2��10-5 | 4��10-5 | 3��10-5 | 2��10-5 |
��3�������£���Na2SO3��Һ����SO2�Ĺ����У�pH��n��SO32-����n��HSO3-���仯���±���
| N��SO32-����n��HSO3-�� | 91��9 | 1��1 | 9��91 |
| pH | 8.2 | 7.2 | 6.2 |
��4����֪��2NO��g��+O2��g��?2NO2��g����H=-113.0kJ•mol-1
2SO2��g��+O2��g��?2SO3��g����H=-196.6kJ•mol-1
��ӦNO2��g��+SO2��g��?SO3��g��+NO��g���ġ�H=-41.8kJ•mol-1��
һ�������£���NO��SO2�������1��2�����ܱ������з���������Ӧ��������˵����Ӧ�ﵽƽ��״̬����b��
a����ϵѹǿ���ֲ��� b�����������ɫ���ֲ��� c��SO3��NO��������ֲ��� d��ÿ����1molSO3��ͬʱ����1molNO2��
| A�� | ̼������ȷֽ� | B�� | �Ҵ�ȼ�� | ||
| C�� | ����������ķ�Ӧ | D�� | ����������ˮ |
| A�� | V��C����V��B��=2��3 | |
| B�� | ��λʱ������nmolA��ͬʱ����3nmolB | |
| C�� | A��B��C������������ٱ仯 | |
| D�� | A��B��C�ķ�������Ϊ1��3��2 |
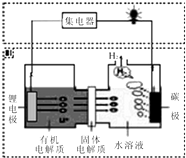 �������ѧ�ҷ�����һ�����Ϳɿص��--�ˮ��أ�����ԭ����ͼ��ʾ�������й�˵������ȷ���ǣ�������
�������ѧ�ҷ�����һ�����Ϳɿص��--�ˮ��أ�����ԭ����ͼ��ʾ�������й�˵������ȷ���ǣ�������| A�� | ̼�������ķ�Ӧ�ǣ�2H2O+2e-=H2��+2OH - | |
| B�� | �л�����ʺ�ˮ��Һ�����Ի������� | |
| C�� | ����²���22.4L������ʱ����������﮵�����Ϊ14g | |
| D�� | ��װ�ò������ṩ���ܣ����ɵõ��������� |
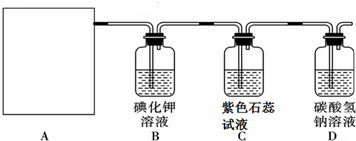
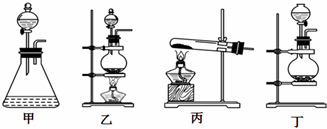
 ������һ����Ҫ���л�����ԭ�ϣ������������������գ�
������һ����Ҫ���л�����ԭ�ϣ������������������գ� $\stackrel{����}{��}$
$\stackrel{����}{��}$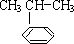 ����Ӧ����Ϊ�ӳɷ�Ӧ
����Ӧ����Ϊ�ӳɷ�Ӧ