题目内容
9.下列说法正确的是( )| A. | 据能量守恒定律,反应物的总能量一定等于生成物的总能量 | |
| B. | 只要有能量的变化,一定发生了化学反应 | |
| C. | 所有的化学反应都有能量变化 | |
| D. | 需要加热才能发生的反应一定是吸热反应 |
分析 A.根据能量守恒定律知,反应物总能量大于生成物总能量,则该反应放出热量,反应物总能量小于生成物总能量,则该反应吸收热量;
B.物理变化中也有能量变化;
C.化学反应中一定伴随着能量变化;
D.需要加热才能进行的反应,不一定是吸热反应.
解答 解:A.化学反应中生成物总能量不等于反应物的总能量,反应前后的能量差值为化学反应中的能量变化,反应物的总能量大于生成物的总能量则为放热反应,否则吸热反应,故A错误;
B.物理变化中也有能量变化,如浓硫酸稀释,物质三态变化等,不发生化学变化,故B错误;
C.化学反应中通常伴随着能量的变化,一般表现为热能,故C正确;
D.需要加热才能进行的反应,不一定是吸热反应,如铝热反应是放热反应,但需在加热条件下以保证足够的热量引发氧化铁和铝粉反应,故D错误.
故选C.
点评 本题考查化学反应的能量变化的定性判断,一个反应是吸热还是放热,关键在于相对能量的大小,与反应的条件无关;

练习册系列答案
 导学教程高中新课标系列答案
导学教程高中新课标系列答案
相关题目
20.关于三种有机物叙述错误的是(-SH的性质类似于-OH)( )


| A. | 都能发生酯化反应 | |
| B. | 都能与NaOH反应 | |
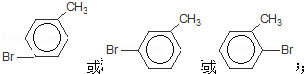
| C. | 甲的苯环上的一氯代物有4种 | |
| D. | 丙的分子式为C10H15ON,能与酸反应 |
4.下列物质与NaOH醇溶液共热完全反应后,可得3种有机物的是( )
| A. | CH3-CHCl-CH2-CH3 | B. | 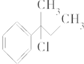 | ||
| C. | CH3-C(CH3)Cl-CH2-CH3 | D. | 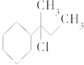 |
14.下列离子中,半径最大的是( )
| A. | S2- | B. | N3- | C. | Cl- | D. | Mg2+ |
1.下表给出几种氢化物的熔点和沸点:
有关表中所列四种氢化物的性质,以下叙述正确的是:( )
①氯化铝在加热时能升华,
②四氯化硅在晶态时属于分子晶体,
③氯化钠晶体中粒子之间以范德华力结合,
④氯化镁的熔沸点比氯化钠低,主要是受堆积方式,键的极性、品格能等影响.
| NaCl | MgCl2 | AlCl3 | SiCl4 | |
| 熔点/℃ | 801 | 714 | 190 | -70 |
| 沸点/℃ | 1 413 | 1 412 | 180 | 57.57 |
①氯化铝在加热时能升华,
②四氯化硅在晶态时属于分子晶体,
③氯化钠晶体中粒子之间以范德华力结合,
④氯化镁的熔沸点比氯化钠低,主要是受堆积方式,键的极性、品格能等影响.
| A. | ② | B. | ③④ | C. | ①②④ | D. | ①②③④ |
18.下列说法正确的是( )
| A. | $\stackrel{235}{92}$U和$\stackrel{238}{92}$U是中子数不同质子数相同的同种核素 | |
| B. | 同种元素的原子均有相同的质子数和中子数 | |
| C. | 质子数为53,中子数为78的碘原子:$\stackrel{131}{53}$I | |
| D. | 通过化学变化可以实现16O与18O间的相互转化 |
 D.CH3-CH2-CH2-CH3和
D.CH3-CH2-CH2-CH3和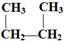 E.液氯和氯气 F.CO(NH2)2和NH4CNOG.C60和金刚石
E.液氯和氯气 F.CO(NH2)2和NH4CNOG.C60和金刚石