题目内容
20.关于三种有机物叙述错误的是(-SH的性质类似于-OH)( )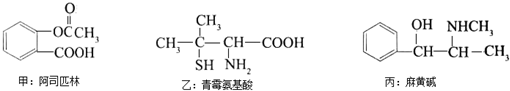
| A. | 都能发生酯化反应 | |
| B. | 都能与NaOH反应 | |
| C. | 甲的苯环上的一氯代物有4种 | |
| D. | 丙的分子式为C10H15ON,能与酸反应 |
分析 A.甲和乙含有羧基、丙含有醇羟基,含有羧基或羟基的物质能发生酯化反应;
B.酯基或羧基、酚羟基都能和NaOH反应;
C.甲苯环上氢原子有4类,有几类氢原子,其一氯代物就有几种;
D.丙的分子式是C10H15ON,丙含有氨基.
解答 解:A.甲和乙含有羧基、丙含有醇羟基,含有羧基或羟基的物质能发生酯化反应,所以三种物质都能发生酯化反应,故A正确;
B.酯基或羧基、酚羟基都能和NaOH反应,丙苯环羧基、酯基或酚羟基,所以不能和NaOH反应,故B错误;
C.甲苯环上氢原子有4类,有几类氢原子,其一氯代物就有几种,所以甲苯环上一氯代物有4种,故C正确;
D.丙的分子式是C10H15ON,丙含有氨基,能和酸反应,故D正确;
故选B.
点评 本题考查有机物结构和性质,为高频考点,把握官能团及其性质关系是解本题关键,侧重考查氨基、羧基和酯基的性质,易错选项是C.

练习册系列答案
 暑假作业暑假快乐练西安出版社系列答案
暑假作业暑假快乐练西安出版社系列答案
相关题目
10.化学源于生活又服务于生活,下列说法正确的是( )
| A. | 淀粉、纤维素、蛋白质、油脂都是天然高分子化合物 | |
| B. | “地沟油”经过加工处理后,可以用来制肥皂和生物柴油 | |
| C. | 变质的油脂有难闻的特殊气味,是由于油脂发生了水解反应 | |
| D. | 医药中常用酒精来消毒,是因为酒精能够使细菌蛋白质发生盐析 |
11.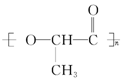 在国际环境问题中,使用一次性聚苯乙烯材料带来的“白色污染”极为严重,因为这种材料难分解,处理麻烦.最近科学家研制出了一种新材料(如图)能代替聚苯乙烯,它是由乳酸(一种有机羟基羧酸)缩聚而成,能在乳酸菌的作用下降解而消除对环境的污染.下列关于聚乳酸的说法正确的是( )
在国际环境问题中,使用一次性聚苯乙烯材料带来的“白色污染”极为严重,因为这种材料难分解,处理麻烦.最近科学家研制出了一种新材料(如图)能代替聚苯乙烯,它是由乳酸(一种有机羟基羧酸)缩聚而成,能在乳酸菌的作用下降解而消除对环境的污染.下列关于聚乳酸的说法正确的是( )
 在国际环境问题中,使用一次性聚苯乙烯材料带来的“白色污染”极为严重,因为这种材料难分解,处理麻烦.最近科学家研制出了一种新材料(如图)能代替聚苯乙烯,它是由乳酸(一种有机羟基羧酸)缩聚而成,能在乳酸菌的作用下降解而消除对环境的污染.下列关于聚乳酸的说法正确的是( )
在国际环境问题中,使用一次性聚苯乙烯材料带来的“白色污染”极为严重,因为这种材料难分解,处理麻烦.最近科学家研制出了一种新材料(如图)能代替聚苯乙烯,它是由乳酸(一种有机羟基羧酸)缩聚而成,能在乳酸菌的作用下降解而消除对环境的污染.下列关于聚乳酸的说法正确的是( )| A. | 聚乳酸是一种纯净物 | |
| B. | 聚乳酸是一种羧酸 | |
| C. | 聚乳酸的单体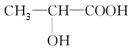 | |
| D. | 其聚合方式与聚苯乙烯的聚合方式相同 |
8.超氧化钾KO2也和过氧化钠一样,吸收CO2变成碳酸盐并放出O2.若有0.5molKO2与过量CO2反应,则产生O2的物质的量为( )
| A. | 0.125mol | B. | 0.375mol | C. | 0.5mol | D. | 0.75mol |
15.下列说法中正确的是( )
| A. | 废旧轮胎均可直接在室外焚烧处理 | |
| B. | 电木可溶于酒精 | |
| C. | 聚氯乙烯属于吸水性高分子树脂 | |
| D. | 复合材料玻璃钢具有强度高、质量轻等优点 |
12.人类将在未来几十年内逐渐由“碳素燃料文明时代”过渡至“太阳能文明时代”(包括风能、生物质能等太阳能的转换形态),届时人们将适应“低碳经济”和“低碳生活”.下列说法不正确的是( )
| A. | 目前研究菠菜蛋白质“发电”不属于“太阳能文明” | |
| B. | 发展太阳能经济有助于减缓温室效应 | |
| C. | 太阳能电池可将太阳能转化为电能 | |
| D. | 石油和天然气都属于碳素燃料 |
9.下列说法正确的是( )
| A. | 据能量守恒定律,反应物的总能量一定等于生成物的总能量 | |
| B. | 只要有能量的变化,一定发生了化学反应 | |
| C. | 所有的化学反应都有能量变化 | |
| D. | 需要加热才能发生的反应一定是吸热反应 |
10.下列物质中既有离子键、又有共价键的是( )
| A. | C60 | B. | CaCl2 | C. | KF | D. | NH4Cl |
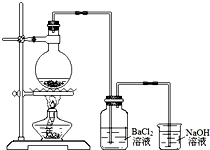 某学习小组探究铜跟浓硫酸反应的情况.取6.4g铜片和10mL 18mol•L-1的浓硫酸放在圆底烧瓶中,按右图所示装置进行实验.
某学习小组探究铜跟浓硫酸反应的情况.取6.4g铜片和10mL 18mol•L-1的浓硫酸放在圆底烧瓶中,按右图所示装置进行实验.