题目内容
8.下列关于合金的说法错误的是( )| A. | 合金是由两种或两种以上的金属与非金属经一定方法所合成的具有金属特性的物质 | |
| B. | 镁铝合金的熔点比镁和铝都髙 | |
| C. | 在合金中加入适量的稀土金属能大大改善其性能 | |
| D. | 青铜、硬铝、钢都是合金 |
分析 A.合金是由两种或两种以上的金属或金属与非金属融合而成的具有金属特性的混合物;
B.合金的熔点低硬度大;
C.在合金中加入适量稀土金属,就能大大改善合金的性能;
D.合金是指在一种金属中加热熔合其它金属或非金属而形成的具有金属特性的物质.
解答 解:A.合金是由两种或两种以上的金属与非金属经一定方法所合成的具有金属特性的物质,故A正确;
B.镁铝合金的熔点比镁和铝都低,故B错误;
C.在合金中加入适量稀土金属或稀土金属的化合物,就能大大改善合金的性能,故C正确;
D.青铜、硬铝、钢都是由两种或两种以上的金属(或金属与非金属)熔合在一起形成的具有金属特性的物质,属于合金,故D正确.
故选B.
点评 本题考查合金,题目难度不大,注意把握相关基础知识的积累,注意合金的熔点比其成分金属都低,而不是在二者之间.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
18.下列说法正确的是( )
| A. | 苯不能使KMnO4溶液褪色,因此苯不能发生氧化反应 | |
| B. | 用溴水鉴别苯和正己烷 | |
| C. | 甲烷和Cl2的反应与乙烯和Br2的反应属于同一类型的反应 | |
| D. | 乙烯和苯都能使溴水褪色,褪色的原因不相同 |
16.下列说法中,不正确的是( )
| A. | SO2(g)+0.5O2(g)?SO3(g)△H=-213kJ•mol-1 说明25℃,101kPa下,lmolSO2与0.5mol氧气放入密闭容器中生成SO3时放出213 kJ热量 | |
| B. | 若反应物总能量高于生成物总能量,反应放热,△H<0 | |
| C. | 化学反应必然伴随能量变化 | |
| D. | 酸和碱的中和反应都是放热反应 |
3.下列烃在光照下与氯气反应,只生成两种一氯代物的有( )
| A. | 甲苯 | B. | 环戊烷 | C. | 2,2-二甲基丁烷 | D. | 对二甲苯 |
20.A、B两个烧杯中分别盛有100mL3.0mol/L的盐酸和烧碱溶液,向两个烧杯中分别加入等质量的Al粉,在相同条件下产生气体的体积比A:B=2:5,则加入铝粉的质量为( )
| A. | 8.1g | B. | 6.75g | C. | 5.4g | D. | 2.7 g |
17.有a、b、c、d四种金属,将a与b用导线连结浸入某电解质溶液中,电流由b经外电路流向a.将a、d分别投入等浓度的盐酸中,d比a反应剧烈.将Cu浸入b的盐溶液里,无明显变化.如果把Cu浸入c的盐溶液里,有c的单质析出,据此判断它们的活动性由强到弱的顺序是( )
| A. | d、a、b、c | B. | b、a、d、c | C. | d、b、a、c | D. | d、c、a、b |
18.生命起源于海洋,科学家认为,由于海洋中Al3+的浓度极低,所以Al元素未成为人体内的必需元素,相反它对人体有害,下列有关铝的说法中不正确的是( )
| A. | 家庭不宜用铝锅长期盛放菜,汤等食品 | |
| B. | 明矾[KAl(SO4)2•12H2O]含结晶水,是混合物 | |
| C. | Al既能与盐酸反应,又能与NaOH溶液反应 | |
| D. | 铝热反应是放热反应 |
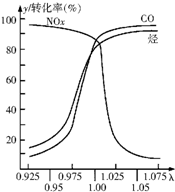 随着经济的发展和生活水平的提高,近年来我省汽车拥有量呈较快增长趋势.
随着经济的发展和生活水平的提高,近年来我省汽车拥有量呈较快增长趋势.