题目内容
【题目】下图是氧气氧化某浓度Fe2+为Fe3+过程的实验结果,下列有关说法正确的是
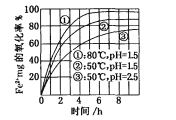
A. pH=1.5时氧化率一定比pH=2.5时大
B. 其他条件相同时,80℃的氧化率比50℃大
C. Fe2+的氧化率仅与溶液的pH和温度有关
D. 该氧化过程的离子方程式为:Fe2++O2+4H+=Fe3++2H2O
【答案】B
【解析】
试题A、由图像分析,亚铁离子的氧化率受温度和pH影响,所以Ph=1.5的氧化率不一定比Ph=2.5时的氧化率大,错误,不选A;B、其它条件相同时温度不同时,亚铁的氧化率与温度成正比,温度越高,氧化率越大,正确,选B;C、亚铁离子的氧化率不仅与溶液的pH有关还与温度有关,还与离子的浓度等其它因素有关,错误,不选C;D、被氧化过程的离子方程式中电荷不守恒,错误,不选D。

【题目】二氯化二硫(S2Cl2)在工业上用于橡胶的硫化。为在实验室合成S2Cl2,某化学研究性学习小组查阅了有关资料,得到如下信息:
①将干燥纯净的氯气在110℃~140℃与硫反应,即可得S2Cl2粗品。
②有关物质的部分性质如下表:
物质 | 熔点/℃ | 沸点/℃ | 化学性质 |
S | 112.8 | 444.6 | 略 |
S2Cl2 | -77 | 137 | 与过量氯气发生S2Cl2+Cl2 |
设计实验装置图如下:

(1)仪器A的名称是______________。
B中反应的离子方程式为_________________________________。
(2) S2Cl2遇水会生成黄色单质、一种能使品红溶液褪色的气体化合物及酸雾,D中的试剂应是________,写出该反应的化学方程式__________________ 。
(3)装置H的作用是_______________ ,其中发生反应的化学方程式为 ______________________。
(4)S2Cl2粗品中可能混有的杂质是SCl2、Cl2、S,为了提高S2Cl2的纯度,关键的操作是控制好温度和_______。