题目内容
下列叙述或操作不正确的是( )
| A、浓硫酸具有强氧化性,稀硫酸无氧化性 |
| B、浓硫酸不慎沾到皮肤上,立即用大量的水冲洗 |
| C、稀释浓硫酸时应将浓硫酸沿着烧杯壁慢慢地注入盛有水的烧杯中,并不断搅拌 |
| D、浓硫酸与碳的反应中,浓硫酸仅表现强氧化性 |
考点:化学实验安全及事故处理
专题:化学实验基本操作
分析:A.反应中元素的化合价降低、被还原的反应为氧化反应,浓硫酸、稀硫酸都具有氧化性;
B.浓硫酸具有很强的腐蚀性,且稀释时会放出大量的热;
C.浓硫酸稀释过程中放出大量热,且浓硫酸密度大于水,据此判断正确的稀释方法;
D.浓硫酸与碳反应生成二氧化碳、二氧化碳和水,根据化合价变化及反应产物可知,浓硫酸只表现了强氧化性.
B.浓硫酸具有很强的腐蚀性,且稀释时会放出大量的热;
C.浓硫酸稀释过程中放出大量热,且浓硫酸密度大于水,据此判断正确的稀释方法;
D.浓硫酸与碳反应生成二氧化碳、二氧化碳和水,根据化合价变化及反应产物可知,浓硫酸只表现了强氧化性.
解答:
解:A.浓硫酸具有强氧化性,稀硫酸能够与活泼金属反应生成氢气,该反应中稀硫酸表现了氧化性,故A错误;
B.浓硫酸具有较强较强的腐蚀性,不慎沾到皮肤上,立即用大量水冲洗会灼伤皮肤,应立即用布拭去,再用大量清水冲洗,故B错误;
C.浓硫酸密度大于水,稀释会放出大量热,所以稀释浓硫酸时应将浓硫酸沿着烧杯壁慢慢地注入盛有水的烧杯中,并不断搅拌,故C正确;
D.浓硫酸与碳发生反应:C+2H2SO4(浓)
CO2↑+2SO2↑+2H2O,生成二氧化硫时S元素的化合价降低,体现其强氧化性,所以浓硫酸仅表现强氧化性,故D正确;
故选AB.
B.浓硫酸具有较强较强的腐蚀性,不慎沾到皮肤上,立即用大量水冲洗会灼伤皮肤,应立即用布拭去,再用大量清水冲洗,故B错误;
C.浓硫酸密度大于水,稀释会放出大量热,所以稀释浓硫酸时应将浓硫酸沿着烧杯壁慢慢地注入盛有水的烧杯中,并不断搅拌,故C正确;
D.浓硫酸与碳发生反应:C+2H2SO4(浓)
| ||
故选AB.
点评:本题考查了化学实验安全事故及处理方法、浓硫酸的性质,题目难度不大,注意掌握化学实验基本操作方法,明确浓硫酸的酸性、强氧化性的判断方法.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
下列金属材料中,最适合制造飞机外壳的是( )
| A、镁铝合金 | B、铜合金 |
| C、碳素钢 | D、钠钾合金 |
关于氮的变化关系图如下:
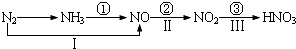
则下列说法正确的是( )

则下列说法正确的是( )
| A、路线①②③是工业生产硝酸的主要途径 |
| B、路线ⅠⅡⅢ是雷电固氮生成硝酸的主要途径 |
| C、上述并不是所有反应都是氧化还原反应 |
| D、上述反应中①②③均属于氮的固定 |
下列离子方程式正确的是( )
| A、氢硫酸与CuSO4溶液混合:S2-+Cu2+═CuS↓ | ||||
| B、磷酸二氢钙溶液跟足量NaOH溶液反应:3Ca2++2H2PO4-+4OH-═Ca3(PO4)2↓+4H2O | ||||
| C、硝酸亚铁溶液中滴入稀硫酸:3Fe2++NO3-+4H+═3Fe3++NO↑+2H2O | ||||
D、电解MgCl2溶液:2H2O+2Cl-
|
下列各组物质中性质的变化规律排列正确的是( )
| A、微粒半径:Al3+>Mg2+>Na+>F- |
| B、稳定性:HI>HBr>HCl>HF |
| C、酸性:HClO4>H2SO4>H3PO4>H4SiO4 |
| D、碱性:Ca(OH)2>KOH>Mg(OH)2>Al(OH)3 |
下列叙述不正确的是( )
| A、NH3易液化,氨常用作制冷剂 |
| B、铝盐和铁盐可以用于净水 |
| C、与金属反应时,稀HNO3可能被还原为更低价态,则稀HNO3氧化性强于浓HNO3 |
| D、淘金者利用密度的不同,用淘洗的方法将金子从沙里分出来 |