题目内容
10.某工业废水中仅含表离子中的5种,且各种离子的物质的量浓度相等.均为0.1mol•L-1.| 阳离子 | K+ Cu2+ Fe3+ Al3+ Fe2+ |
| 阴离子 | Cl- CO32- NO3- SO42- SiO32- |
I.用铂丝蘸取少量溶液液,在火焰上灼烧,无紫色火焰(透过蓝色钴玻璃观察).
Ⅱ.取少溶液,加入KSCN溶液无明显变化.
Ⅲ.另取溶液加入少量盐酸,有无色气体生成,该无色气体遇空气变成红棕色,此时溶液依然澄淸.且溶液中阴离子种类不变.
Ⅳ.向Ⅲ中听得的溶液中加入BaCl2溶液,有白色沉淀生成.
(1)仅由I、Ⅱ判断,溶液中一定不含有的阳离子是K+、Fe3+ (写离子符号).
(2)将Ⅲ中所得红棕色气体通人水中,气体变无色,所发生的化学方程式为:3NO2+H2O═2HNO3+NO.
(3)原溶液中所含阳离子是Fe2+、Cu2+,阴离子是Cl-、NO3-、SO42-.(写离子符号)
分析 Ⅰ.用铂丝蘸取少量溶液,在火焰上灼烧,无紫色火焰(透过蓝色钴玻璃观察),说明没有K+.
Ⅱ.取少量溶液,加入KSCN溶液无明显变化,说明没有Fe3+.
Ⅲ.另取溶液加入少量盐酸,有无色气体生成,该无色气体遇空气变成红棕色,此时溶液依然澄清,且溶液中阴离子种类不变,说明 Fe2+与NO3-和H+反应生成NO,即溶液中有Fe2+、NO3-,加盐酸溶液中阴离子种类不变,说明原溶液中有Cl-,加盐酸溶液依然澄清加盐酸说明没有SiO32-;
Ⅳ.向Ⅲ中所得的溶液中加入BaCl2溶液,有白色沉淀生成,说明有SO42-;根据以上判断分析.
解答 解:Ⅰ.用铂丝蘸取少量溶液,在火焰上灼烧,无紫色火焰(透过蓝色钴玻璃观察),说明没有K+.
Ⅱ.取少量溶液,加入KSCN溶液无明显变化,说明没有Fe3+.
Ⅲ.另取溶液加入少量盐酸,有无色气体生成,该无色气体遇空气变成红棕色,此时溶液依然澄清,且溶液中阴离子种类不变,说明 Fe2+与NO3-和H+反应生成NO,即溶液中有Fe2+、NO3-,加盐酸溶液中阴离子种类不变,说明原溶液中有Cl-,加盐酸溶液依然澄清加盐酸说明没有SiO32-;
Ⅳ.向Ⅲ中所得的溶液中加入BaCl2溶液,有白色沉淀生成,说明有SO42-;
(1)由Ⅰ、Ⅱ判断,溶液中一定不含有的阳离子是K+、Fe3+,
故答案为:K+、Fe3+;
(2)NO2气体和水反应得到的硝酸和一氧化氮,反应为:3NO2+H2O═2HNO3+NO;故答案为:3NO2+H2O═2HNO3+NO;
(3)由以上推断可知溶液中阴离子为 Cl-、NO3-、SO42-,且各为0.1mol/L;已经推断出的阳离子是Fe2+,其浓度为0.1mol/L,由电荷守恒可知溶液中还有一种+2价阳离子,所以还有Cu2+,所以甲同学最终确定原溶液中所含阳离子是:Fe2+、Cu2+;阴离子是:Cl-、NO3-、SO42-;
故答案为:Fe2+、Cu2+;Cl-、NO3-、SO42-.
点评 本题考查离子的检验,侧重考查学生的分析能力和计算能力,注意把握离子的性质以及实验现象的判断,难度不大.

| 选项 | 实验操作及现象 | 实验结论 |
| A | 向某溶液中加入盐酸酸化的氯化钡溶液,有白色沉淀生成 | 该溶液中一定含有SO42- |
| B | 向某溶液中滴加NaOH溶液,产生白色沉淀 | 该溶液中一定含有Al3+ |
| C | 向某溶液中加人NaOH浓溶液,加热,产生的气体能使湿润的 红色石蕊试纸变蓝 | 该溶液中一定含有NH4+ |
| D | 向某紫红色溶液中加人过量Na2SO3溶液,溶液紫红色褪去 | 该溶液中一定含有MnO4- |
| A. | A | B. | B | C. | C | D. | D |
| 选项 | 被提纯的物质 | 除杂试剂 | 分离方法 |
| A | 乙酸乙酯(乙酸) | CCl4 | 萃取、分液 |
| B | 苯(苯酚) | 浓溴水 | 过滤 |
| C | 乙烷(乙烯) | 酸性高锰酸钾溶液 | 洗气 |
| D | 溴苯(溴) | 氢氧化钠溶液 | 分液 |
| A. | A | B. | B | C. | C | D. | D |
已知:
 (a、b、c均大于零)
(a、b、c均大于零)下列说法不正确的是( )
| A. | 反应物的总能量高于生成物的总能量 | |
| B. | 断开1molH-H键和1molI-I键所需能量大于断开2molH-I键所需能量 | |
| C. | 断开2molH-I键所需能量约为(c+b+a)kJ | |
| D. | 向密闭容器中加入2molH2和2molI2,充分反应放出的热量大小2akJ |
| A. | v(A)=0.4mol•L-1•s-1 | B. | v(B)=0.4 mol•L-1•s-1 | ||
| C. | v(C)=0.9 mol•L-1•s-1 | D. | v(D)=1 mol•L-1•s-1 |
| A. | 将SO2通入Ca(ClO)2溶液:Ca2++2ClO-+SO2+H2O=CaSO3↓+2HClO | |
| B. | NaHCO3溶液中滴入少量澄清石灰水:HCO3-+Ca2++OH-=CaCO3↓+H2O | |
| C. | 用氨水吸收过量二氧化硫:2NH3•H2O+SO2=2NH4++SO32-+H2O | |
| D. | 饱和Na2CO3溶液中通入足量CO2:2Na++H2O+CO2+CO32-=2NaHCO3↓ |
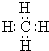 ,AxByCz的分子式AlC3H9.
,AxByCz的分子式AlC3H9.