题目内容
19.在2A+B?3C+4D反应中,表示该反应速率最快的是( )| A. | v(A)=0.4mol•L-1•s-1 | B. | v(B)=0.4 mol•L-1•s-1 | ||
| C. | v(C)=0.9 mol•L-1•s-1 | D. | v(D)=1 mol•L-1•s-1 |
分析 反应速率与化学计量数成正比,则反应速率与化学计量数的比值越大,反应速率越快,以此来解答.
解答 解:反应速率与化学计量数的比值越大,反应速率越快,则
A.$\frac{0.4}{2}$=0.2;
B.$\frac{0.4}{1}$=0.4;
C.$\frac{0.9}{3}$=0.3;
D.$\frac{1}{4}$=0.25,
显然B中反应速率最快,
故选B.
点评 本题考查化学反应速率的比较,为高频考点,把握化学反应速率与化学计量数的关系为解答的关键,侧重分析与应用能力的考查,注意比值法应用及速率单位统一,题目难度不大.

练习册系列答案
 智能训练练测考系列答案
智能训练练测考系列答案
相关题目
9. 298K时,分别向体积、浓度均为20mL0.1mol•L-1的HX溶液、HY溶液中滴加等浓度的NaOH 溶液,混合溶液的pH与加入NaOH溶液体积(V)之间的关系如图所示.(注明:弱电解质的电离度等于已电离的电解质的量与电解质总量之比)下列说法正确的是( )
298K时,分别向体积、浓度均为20mL0.1mol•L-1的HX溶液、HY溶液中滴加等浓度的NaOH 溶液,混合溶液的pH与加入NaOH溶液体积(V)之间的关系如图所示.(注明:弱电解质的电离度等于已电离的电解质的量与电解质总量之比)下列说法正确的是( )
 298K时,分别向体积、浓度均为20mL0.1mol•L-1的HX溶液、HY溶液中滴加等浓度的NaOH 溶液,混合溶液的pH与加入NaOH溶液体积(V)之间的关系如图所示.(注明:弱电解质的电离度等于已电离的电解质的量与电解质总量之比)下列说法正确的是( )
298K时,分别向体积、浓度均为20mL0.1mol•L-1的HX溶液、HY溶液中滴加等浓度的NaOH 溶液,混合溶液的pH与加入NaOH溶液体积(V)之间的关系如图所示.(注明:弱电解质的电离度等于已电离的电解质的量与电解质总量之比)下列说法正确的是( )| A. | 298K 时,0.1mol•L-1HX 溶液中HX的电离度为1% | |
| B. | V=10mL时,同时微热溶液(忽略体积变化),$\frac{c({X}^{-})}{c({Y}^{-})}$逐渐增大 | |
| C. | V=20mL 时,HX曲线对应的溶液中c(Na+)=c(X-)>c(H+)=c(OH-) | |
| D. | 滴定这两种溶液时都可以选择甲基橙替代酚酞作指示剂 |
10.某工业废水中仅含表离子中的5种,且各种离子的物质的量浓度相等.均为0.1mol•L-1.
欲探究废水的组成,进行如下实验:
I.用铂丝蘸取少量溶液液,在火焰上灼烧,无紫色火焰(透过蓝色钴玻璃观察).
Ⅱ.取少溶液,加入KSCN溶液无明显变化.
Ⅲ.另取溶液加入少量盐酸,有无色气体生成,该无色气体遇空气变成红棕色,此时溶液依然澄淸.且溶液中阴离子种类不变.
Ⅳ.向Ⅲ中听得的溶液中加入BaCl2溶液,有白色沉淀生成.
(1)仅由I、Ⅱ判断,溶液中一定不含有的阳离子是K+、Fe3+ (写离子符号).
(2)将Ⅲ中所得红棕色气体通人水中,气体变无色,所发生的化学方程式为:3NO2+H2O═2HNO3+NO.
(3)原溶液中所含阳离子是Fe2+、Cu2+,阴离子是Cl-、NO3-、SO42-.(写离子符号)
| 阳离子 | K+ Cu2+ Fe3+ Al3+ Fe2+ |
| 阴离子 | Cl- CO32- NO3- SO42- SiO32- |
I.用铂丝蘸取少量溶液液,在火焰上灼烧,无紫色火焰(透过蓝色钴玻璃观察).
Ⅱ.取少溶液,加入KSCN溶液无明显变化.
Ⅲ.另取溶液加入少量盐酸,有无色气体生成,该无色气体遇空气变成红棕色,此时溶液依然澄淸.且溶液中阴离子种类不变.
Ⅳ.向Ⅲ中听得的溶液中加入BaCl2溶液,有白色沉淀生成.
(1)仅由I、Ⅱ判断,溶液中一定不含有的阳离子是K+、Fe3+ (写离子符号).
(2)将Ⅲ中所得红棕色气体通人水中,气体变无色,所发生的化学方程式为:3NO2+H2O═2HNO3+NO.
(3)原溶液中所含阳离子是Fe2+、Cu2+,阴离子是Cl-、NO3-、SO42-.(写离子符号)
7.某同学将铁片A和碳棒B用导线连接后放入食盐水中模拟菜刀生锈过程,则下列叙述错误的是( )
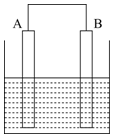

| A. | 导线中有电子流动,电流方向为A流向B | |
| B. | 溶液中的O2在电极B得电子,电极B附近碱性增强 | |
| C. | 电极A上的电极反应式为Fe-2e-=Fe2+ | |
| D. | 溶液中的Na+向电极B附近移动 |
14.下列各装置能够构成原电池的是( )
| A. |  | B. |  | ||
| C. |  | D. |  |
4.乙炔和电石(CaC2)都是重要的化工原料.
(1)电石可由焦炭与氧化钙固体在电炉中高温制得,同时生成一氧化碳气体.
①每生成1.00g固态CaC2吸收7.25kJ的热量,该制备反应的热化学方程式为CaO(s)+3C(s)$\frac{\underline{\;高温\;}}{\;}$CaC2(s)+CO(g)△H=+464kJ/mol
②CaC2与H2O反应的化学方程式为CaC2+2H2O=Ca(OH)2+HC≡CH↑
③炼钢时可用电石将钢水中FeO转变为铁,同时有一氧化碳等物质生成,该反应的化学方程式为3FeO+CaC2$\frac{\underline{\;高温\;}}{\;}$3Fe+CaO+2CO↑
(2)已知下列反应:
CH4 (g)+2O2(g)═CO2(g)+2H2O(g)△H1=akJ•mol-1
2C2H2(g)+5O2(g)═4CO2(g)+2H2O(g)△H2=bkJ•mol-1
2H2(g)+O2(g)═2H2O(g)△H3=ckJ•mol-1
2CH4(g)═C2H2(g)+3H2(g)△H4
①△H4=$\frac{4a-b-3c}{2}$kJ•mol-1(用含a、b、c的代数式表示).
②已知下列键能数据:
则△H4=+360.4kJ•mol-1(填数值).
(3)在压强为1×105kPa的恒压密闭容器中充入1mol乙炔和1molHCl气体,加入催化剂,乙炔与HCl发生反应:HC≡CH(g)+HCl(g)?CH2=CHCl(g),乙炔的平衡转化率与温度的关系如图所示:

①该反应的△H<0(填“>”或“<”),N点时乙炔的反应速率v(正)>v(逆) (填“>”、“<”或“=”).
②M点对应温度的平衡常数Kp=9.9×10-4(kPa)-1(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数,并注明单位)
(1)电石可由焦炭与氧化钙固体在电炉中高温制得,同时生成一氧化碳气体.
①每生成1.00g固态CaC2吸收7.25kJ的热量,该制备反应的热化学方程式为CaO(s)+3C(s)$\frac{\underline{\;高温\;}}{\;}$CaC2(s)+CO(g)△H=+464kJ/mol
②CaC2与H2O反应的化学方程式为CaC2+2H2O=Ca(OH)2+HC≡CH↑
③炼钢时可用电石将钢水中FeO转变为铁,同时有一氧化碳等物质生成,该反应的化学方程式为3FeO+CaC2$\frac{\underline{\;高温\;}}{\;}$3Fe+CaO+2CO↑
(2)已知下列反应:
CH4 (g)+2O2(g)═CO2(g)+2H2O(g)△H1=akJ•mol-1
2C2H2(g)+5O2(g)═4CO2(g)+2H2O(g)△H2=bkJ•mol-1
2H2(g)+O2(g)═2H2O(g)△H3=ckJ•mol-1
2CH4(g)═C2H2(g)+3H2(g)△H4
①△H4=$\frac{4a-b-3c}{2}$kJ•mol-1(用含a、b、c的代数式表示).
②已知下列键能数据:
| 共价键 | C-H | H-H | C≡C |
| 键能/kJ•mol-1 | 413.4 | 436 | 812 |
(3)在压强为1×105kPa的恒压密闭容器中充入1mol乙炔和1molHCl气体,加入催化剂,乙炔与HCl发生反应:HC≡CH(g)+HCl(g)?CH2=CHCl(g),乙炔的平衡转化率与温度的关系如图所示:

①该反应的△H<0(填“>”或“<”),N点时乙炔的反应速率v(正)>v(逆) (填“>”、“<”或“=”).
②M点对应温度的平衡常数Kp=9.9×10-4(kPa)-1(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数,并注明单位)
8.下列科学家与其科学成果对应关系正确的是( )
| A. | 道尔顿:分子学说 | B. | 汤姆生:射线的发现 | ||
| C. | 卢瑟福:原子结构的行星模型 | D. | 伦琴:原子的葡萄干面包模型 |
10.对下列化工生产认识正确的是( )
| A. | 制备硫酸:使用热交换器可以充分利用能量 | |
| B. | 侯德榜制碱:析出NaHCO3的母液中加入消石灰,可以循环利用NH3 | |
| C. | 合成氨:采用500℃的高温,有利于增大反应正向进行的程度 | |
| D. | 合成氯化氢:通入H2的量略大于Cl2,可以使平衡正移 |

 +(2n-1)H2O.
+(2n-1)H2O.