题目内容
10.有X、Y、Z和W四种元素.已知:①X、Y、Z属同一短周期,其离子以X2+、Y3+、Z-的形式存在.②W和Z组成化合物WZ3溶液遇苯酚呈紫色.请回答:(1)Z的最高价氧化物对应水化物的名称为高氯酸.
(2)X的单质在二氧化碳中燃烧的化学方程式为2Mg+CO2$\frac{\underline{\;点燃\;}}{\;}$2MgO+C.
(3)Y的单质可用于冶炼金属锰,写出Y与二氧化锰反应的化学方程式3MnO2+4Al$\frac{\underline{\;高温\;}}{\;}$2Al2O3+3Mn,
Y的最高价氧化物对应的水化物既可溶于强酸又可溶于强碱,请用电离平衡理论解释其原因在氢氧化铝中存在电离平衡H2O+AlO2-+H+?Al(OH)3?Al3++3OH-,当加入强酸时电离平衡向右移动,氢氧化铝溶解;当加入强碱时电离平衡向左移动,氢氧化铝溶解.
(4)当有28.0g W组成的单质,在加热条件下与足量水完全反应,则生成气体标准状况下的体积为14.9L.
(5)我国陆地上冶炼X的主要流程如图所示
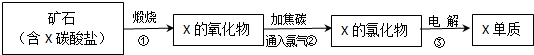
已知当有 lmolX的氧化物参加反应时,有2mol电子转移且生成三种产物,则步骤②反应的化学方程式为3MgO+3Cl2+2C=3MgCl2+CO2+CO.
分析 W和Z组成化合物WZ3溶液遇苯酚呈紫色,则W为Fe,Z为Cl;X、Y、Z属同一短周期,其离子以X2+、Y3+、Z-的形式存在,则X为Mg,Y为Al;
(1)根据氯元素的最高化合价来分析对应的酸;
(2)镁与二氧化碳反应生成氧化镁和碳;
(3)由铝热反应原理来书写化学反应,利用电离平衡移动来解释氢氧化铝既可溶于强酸又可溶于强碱;
(4)由铁和水蒸气反应的方程式来计算;
(5)由步骤可知氧化镁与碳、氯气反应,利用电子的转移数目来分析产物,并书写反应方程式.
解答 解:W和Z组成化合物WZ3溶液遇苯酚呈紫色,则W为Fe,Z为Cl;X、Y、Z属同一短周期,其离子以X2+、Y3+、Z-的形式存在,则X为Mg,Y为Al;
(1)因氯元素的最高化合价为+7价,则对应的最高价氧化物对应水化物为HClO4,其名称为高氯酸,故答案为:高氯酸;
(2)因镁与二氧化碳反应生成氧化镁和碳,反应为2Mg+CO2$\frac{\underline{\;点燃\;}}{\;}$2MgO+C,故答案为:2Mg+CO2$\frac{\underline{\;点燃\;}}{\;}$2MgO+C;
(3)铝与二氧化锰反应生成氧化铝和锰,其反应为3MnO2+4Al$\frac{\underline{\;高温\;}}{\;}$2Al2O3+3Mn,由电离平衡H2O+AlO2-+H+?Al(OH)3?Al3++3OH-,可知加强酸或强碱时都能使氢氧化铝溶解,
故答案为:3MnO2+4Al$\frac{\underline{\;高温\;}}{\;}$2Al2O3+3Mn;在氢氧化铝中存在电离平衡H2O+AlO2-+H+?Al(OH)3?Al3++3OH-,当加入强酸时电离平衡向右移动,氢氧化铝溶解;当加入强碱时电离平衡向左移动,氢氧化铝溶解;
(4)28.0gFe的物质的量为$\frac{28.0g}{56g/mol}$=0.5mol,由3Fe+4H20$\frac{\underline{\;高温\;}}{\;}$Fe3O4+4H2,则氢气的物质的量为$\frac{0.5mol×4}{3}$,其标况下的体积为$\frac{2}{3}$mol×22.4L/mol=14.9L,故答案为:14.9;
(5)由流程图中的反应②可知,氧化镁与碳和氯气反应生成氯化镁和碳的氧化物,lmolMgO参加反应时,有2mol电子转移且生成三种产物,即1mol氯气作氧化剂时,$\frac{2}{3}$mol碳作还原剂,且生成均为$\frac{1}{3}$mol的CO2和CO,其反应为3MgO+3Cl2+2C=3MgCl2+CO2+CO,
故答案为:3MgO+3Cl2+2C=3MgCl2+CO2+CO.
点评 本题考查学生利用物质的检验及物质原子在周期表中的位置来推断元素,然后利用元素化合物知识结合习题中的信息来解答,明确信息的使用及挖掘是解答本题的关键.

| A. | 纯碱溶液清洗油污,加热可增强其去污能力 | |
| B. | 门窗玻璃、陶瓷餐具、玛瑙手镯、砖瓦所用材料为硅酸盐材料 | |
| C. | 聚丙烯酸钠是一种高吸水性树脂 | |
| D. | 汽油、煤油、植物油都是油,但它们的主要成分不相同 |
| A. | 按系统命名法,化合物  的名称为2,6-二甲基-5-乙基庚烷 的名称为2,6-二甲基-5-乙基庚烷 | |
| B. | 符合分子式为C3H4Cl2的所有同分异构体数目为7种 | |
| C. | 丁烷、正戊烷、新戊烷、已烷的沸点依次升高 | |
| D. | 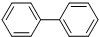 、 、 分别叫做联苯和二苯甲烷,互为同系物,两种分子的所有原子都有可能共平面 分别叫做联苯和二苯甲烷,互为同系物,两种分子的所有原子都有可能共平面 |
| A. | ${\;}_{8}^{16}$O、${\;}_{8}^{17}$O、${\;}_{8}^{18}$O互为同素异形体 | |
| B. | O2和O3互为同位素 | |
| C. | CH3-CH2-CH2-CH3与 互为同系物 互为同系物 | |
| D. |  与 与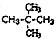 互为同分异构体 互为同分异构体 |
| A. |  2-乙基丙烷 2-乙基丙烷 | B. | CH3CH2CH2OH 1-丁醇 | ||
| C. |  对二甲苯 对二甲苯 | D. | 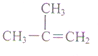 2-甲基-2-丙烯 2-甲基-2-丙烯 |
| A. | 在标准状况下,22.4LCH4与18gH2O所含有的电子数均为10NA | |
| B. | 2.4g金属镁变为镁离子时失去的电子数为0.1NA | |
| C. | 1molHCl气体中的粒子数与0.5 mo1/L盐酸中溶质粒子数相等 | |
| D. | CO和N2为等电子体,22.4L的CO气体与lmol N2所含的电子数相等 |


 .
.