题目内容
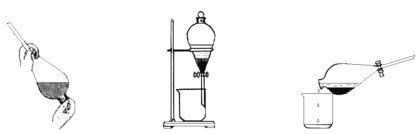
【题目】某同学利用如图所示的装置,验证氨气的喷泉实验。回答下列问题:
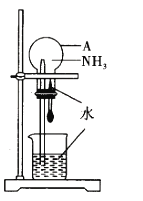
(1)仪器A的名称是_________________。
(2)写出实验室用NH4Cl和Ca(OH)2制氨气的化学方程式:___________________。
(3)喷泉实验前需要在仪器A中充满干燥的氨气。
①可用向____________填“上”或“下”)排空气法收集氨气。
②下列物质可用于干燥氨气的是__________(填序号)。
A. 浓硫酸 B. 碱石灰 C. 浓硝酸
(4)NH3能在水中进行喷泉实验的原因是__________________。
【答案】圆底烧瓶 2 NH4Cl + Ca(OH)2 ![]() CaCl2+ 2 NH3↑+ 2 H2O 下
CaCl2+ 2 NH3↑+ 2 H2O 下
B NH3极易溶于水,使烧瓶内外瞬间产生压强差
【解析】
(1)根据装置特点,仪器A的名称为圆底烧瓶;
(2)实验室用NH4Cl和Ca(OH)2在加热的条件下生成氯化钙、氨气和水,方程式为2 NH4Cl+Ca(OH)2 ![]() CaCl2+2NH3↑+2H2O;
CaCl2+2NH3↑+2H2O;
(3)①氨气的密度比空气小,可采用瓶口向下的方法收集;
②碱石灰不与氨气反应,且能吸收水,可干燥氨气;浓硫酸、浓硝酸均与氨气反应,不能干燥氨气,答案为B。
(4)NH3极易溶于水,氨气溶于水后,在装置内产生压强差,导致烧杯中的水迅速进入烧瓶,形成喷泉。

练习册系列答案
相关题目