题目内容
把一块镁铝合金投入到1 mol·L-1盐酸中,待合金完全溶解后,再往溶液里加入1 mol·L-1 NaOH溶液,生成沉淀的物质的量随加入NaOH溶液体积变化的关系如图所示。下列说法中错误的是( )
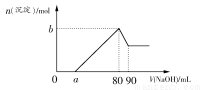
A.盐酸的体积为80 mL
B.a的取值范围为0<a<50
C.n(Mg2+)<0.025 mol
D.当a值为30时,b值为0.01
D
【解析】从开始到沉淀量最大的过程中,涉及的反应有Mg+2H+=Mg2++H2↑、2Al+6H+=2Al3++3H2↑、H++OH-=H2O、Mg2++2OH-=Mg(OH)2↓、Al3++3OH-=Al(OH)3↓,此时消耗的NaOH的物质的量等于HCl的总物质的量,A正确;80 mL~90 mL的NaOH溶液用于溶解Al(OH)3:Al(OH)3+OH-=AlO2-+2H2O,故形成Al(OH)3沉淀消耗NaOH溶液的体积是30 mL,所以a<50,B项正确;从题图来看,若a=0,则Mg2+的最大值是0.025 mol,而a≠0,故C正确;当a为30时,得到Mg(OH)2、Al(OH)3沉淀的物质的量均为0.01 mol,共0.02 mol,D项不正确。

 阳光课堂课时优化作业系列答案
阳光课堂课时优化作业系列答案北京市场销售的某种食用精制盐包装袋上有如下说明:
产品标准 | GB5461 |
产品等级 | 一级 |
配料 | 食盐、碘酸钾、抗结剂 |
碘含量(以I计) | 20~50 mg/kg |
(1)碘酸钾与碘化钾在酸性条件下发生如下反应,配平化学方程式
__________KIO3+__________KI+__________H2SO4=__________K2SO4+__________I2+__________H2O
(2)上述反应生成的I2可用四氯化碳检验。向碘的四氯化碳溶液中加入Na2SO3 稀溶液,将I2 还原,以回收四氯化碳。
①Na2SO3稀溶液与I2反应的离子方程式是__________________。
②某学生设计回收四氯化碳的操作步骤为:
a.将碘的四氯化碳溶液置于分液漏斗中;
b.加入适量Na2SO3稀溶液;
c.分离出下层液体。
以上设计中遗漏的操作及在上述步骤中的位置是__________________。
(3)已知:I2+2S2O32-=2I-+S4O62-。某学生测定食用精制盐的碘含量,其步骤为:
a.准确称取w g食盐,加适量蒸馏水使其完全溶解;
b.用稀硫酸酸化所得溶液,加入足量KI溶液,使KIO3与KI反应完全;
c.以淀粉溶液为指示剂,逐滴向上述溶液中加入物质的量浓度为 2.0×10-3mol/L 的Na2S2O3溶液10.0 mL,恰好反应完全。
①判断c中反应恰好完全依据的现象是__________;
②b中反应所产生的I2的物质的量是__________mol。