题目内容
【题目】在容积为2.0 L的密闭容器内,物质D在T ℃时发生反应,其反应物和生成物的物质的量随时间t的变化关系如图,下列叙述不正确的是
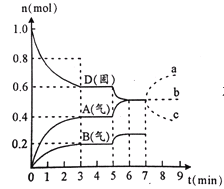
A. 从反应开始到第一次达到平衡时,A物质的平均反应速率为0.0667 mol/(L·min)
B. 该反应的化学方程式为2D(s) 2A(g)+B(g),该反应的平衡常数表达式为K=c(A)2·c(B)
C. 已知:反应的H>0,则第5分钟时图象呈现上述变化的原因可能是升高体系的温度
D. 若在第7分钟时增加D的物质的量,则表示A的物质的量变化正确的是a曲线
【答案】D
【解析】
A.根据v=c/t计算得A物质的平均反应速率为0.4/(2×3)= 0.0667 mol/(L·min),A正确;
B.根据图在第一次达到平衡时A的物质的量增加了0.4mol,B的物质的量增加了0.2mol,所以A、B为生成物,D的物质的量减少了0.4mol/L,所以D为反应物,D、A、B的变化量之比为0.4:0.4:0.2=2:2:1,反应中各物质计量数之比等于物质的浓度的变化量之比,化学方程式为2D(s)![]() 2A(g)+B(g),该反应的平衡常数表达式为K=c(A)2·c(B) ,故B正确;
2A(g)+B(g),该反应的平衡常数表达式为K=c(A)2·c(B) ,故B正确;
C.第5分钟时A、B的物质的量在原来的基础上增加,而D的物质的量在原来的基础上减小,说明平衡正向移动,因为反应的H>0,所以此时是升高温度,故C正确;
D.因为D是固体,量的改变不影响化学平衡,所以A的物质的量不变,故D错误;
综上所述,本题选D。

练习册系列答案
 99加1领先期末特训卷系列答案
99加1领先期末特训卷系列答案 百强名校期末冲刺100分系列答案
百强名校期末冲刺100分系列答案 好成绩1加1期末冲刺100分系列答案
好成绩1加1期末冲刺100分系列答案 金状元绩优好卷系列答案
金状元绩优好卷系列答案
相关题目