题目内容
【题目】下图是一种正投入生产的大型蓄电系统。放电前,被膜隔开的电解质为Na2S2和NaBr3,放电后分别变为Na2S4和NaBr。下列叙述正确的是
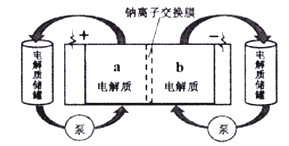
A. 放电时,负极反应为3NaBr-2e-==NaBr3+2Na+
B. 充电时,阳极反应为2Na2S2-2e-== Na2S4+2Na+
C. 放电时,Na+经过离子交换膜,由b池移向a池
D. 用该电池电解饱和食盐水,产生2.24LH2时,b池生成17.40g Na2S4
【答案】C
【解析】放电前,被膜隔开的电解质为Na2S2(右罐)和NaBr3(左罐),则Na2S2在负极失电子,NaBr3在正极得电子;充电时,阴极为负极的逆反应,阳极为正极的逆反应;A.放电时,负极Na2S2失电子,则负极的电极反应式为:2S22--2e-═S42-,故A错误;B.充电时,阳极上Br-失电子转化为Br3-,则阳极的电极反应式为:3Br--2e-=Br3-,故B错误;C.电池放电时,Na2S2和NaBr3反应,则电池的总反应方程式为:2Na2S2+NaBr3=Na2S4+3NaBr,Na+经过离子交换膜,由b池移向a池,故C正确;D. 用该电池电解饱和食盐水,产生2.24LH2时,此气体不是标准状况下的体积,无法进行换算,则b池生成Na2S4的质量不一定是17.40g,故D错误.答案选C。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目