题目内容
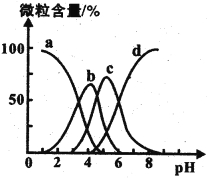
【题目】室温时,CaCO3在水中的沉淀溶解平衡曲线如图所示.已知CaCO3的溶度积(室温)为2.8×10-9,下列说法中不正确的是

A. x的数值为![]()
B. c点时有![]() 生成
生成
C. 加入蒸馏水可使溶液由d点变成a点
D. b点与d点对应的溶度积相等
【答案】C
【解析】
CaCO3在水中的沉淀溶解平衡为CaCO3(s)Ca2+(aq)+CO32-(aq),图象中位于曲线上的b、d点为饱和溶液,处于溶解平衡状态,a点处离子浓度小于饱和溶液浓度为不饱和溶液,c点为过饱和溶液,以此解答该题。
A.在d点c(CO32-)=1.4×10-4mol/L,因室温时,CaCO3的溶度积Ksp=2.8×10-9,所以c(Ca2+)=2×10-5mol/L,故x的数值为2×10-5,故A正确;
B.在c点c(Ca2+)>2×10-5mol/L,即相当于增大c(Ca2+),平衡左移,有CaCO3生成,故B正确;
C.d点为饱和溶液,加入蒸馏水后如仍为饱和溶液,则c(Ca2+)、c(CO32-)都不变,如为不饱和溶液,则二者浓度都减小,故不可能使溶液由d点变成a点,故C错误;
D.b点与d点在相同的温度下,溶度积相等,故D正确。
故选C。

练习册系列答案
 小夫子全能检测系列答案
小夫子全能检测系列答案
相关题目