题目内容
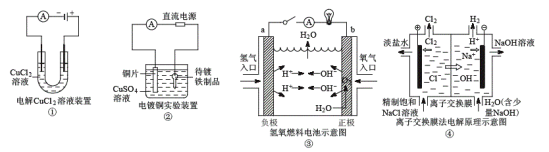
【题目】某校化学小组学生利用如图装置进行“氨的催化氧化及检验产物”实验(图中夹持装置已略去)。下列推断合理的是( )
A.C不需要持续加热
B.D的作用是干燥气体
C.B是无用装置
D.仅用该套装置和药品无法达到检验产物的目的
【答案】AD
【解析】
浓氨水易挥发,鼓入空气将挥发的浓氨水吹入B装置,B中的碱石灰用来干燥氨气,干燥的氨气在C中发生催化氧化生成一氧化氮和水,用浓硫酸吸收生成的水和剩余的氨,剩余干燥的一氧化氮在E中遇到空气发生氧化反应生成红棕色的二氧化氮,二氧化氮与F中的水生成硝酸,溶液显酸性,能够使石蕊变红色,最后用氢氧化钠溶液吸收过量的二氧化氮,据此解答。
A. 氨气的催化氧化为放热反应,放出的热量能够维持反应继续进行,铂丝不需要持续加热;故A正确;
B. 装置B的作用为干燥氨气,装置D的作用不是用来干燥气体,而是通过浓硫酸质量的变化检验水的生成,但装置D中的浓硫酸除了能够吸收水外,还能吸收未参加反应的氨气,故B错误;
C. 装置B的作用为干燥氨气,故C错误;
D. 不能通过D装置增重得出结论反应生成水,一氧化氮为无色,而一氧化氮容易被氧化为红棕色的二氧化氮,所以也不能通过颜色断定氨气的催化氧化生成的氮氧化物,故D正确;
推断合理的是AD。

 课时训练江苏人民出版社系列答案
课时训练江苏人民出版社系列答案 黄冈经典趣味课堂系列答案
黄冈经典趣味课堂系列答案 启东小题作业本系列答案
启东小题作业本系列答案【题目】氮的氧化物是严重的大气污染物,可以通过以下方法处理:
Ⅰ.催化还原法:如在汽车排气管上安装一个催化转化器,发生如下反应: 2NO(g)+2CO(g)N2(g)+2CO2(g)
(1)已知N2(g)+O2(g)2NO(g) △H=+180kJ/mol
化学键 | O=O | C=O | C≡O |
键能(kJ/mol) | 497 | 803 | 1072 |
则反应:2NO(g)+2CO(g) N2(g)+2CO2(g) △H=_____kJ/mol。
(2)在一定温度下,向体积为1L的密闭容器中充入2molNO、1molCO,10分钟时反应2NO(g)+2CO(g)N2(g)+2CO2(g)达到平衡状态,反应过程中反应物浓度随时间变化情况如图所示:
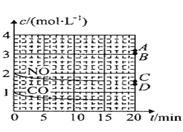
①该反应的平衡常数 K 的计算式为_____;前 10 分钟内用氮气表示的反应速率为_____。
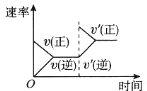
②若保持温度不变,15 分钟时再向该容器中充入1.6molNO、0.4molCO2,则此时反应的ν正______ν逆(填“>”、“=”或“<”)。
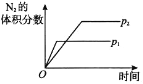
③若保持其他条件不变,15min 时压缩容器的体积至 0.5L,20 分钟时反应重新达到平衡,NO 的浓度对应的点应是图中的_____(填字母)。
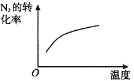
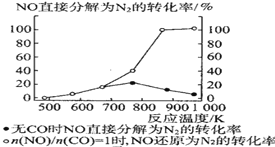
④某科研小组研究发现以 Ag-ZSM-5 为催化剂,NO 转化为 N2 的转化率随温度变化情况如图所示。若不使用 CO,温度超过775K,发现NO的分解率降低,其可能的原因是__________________
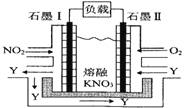
Ⅱ.利用电化学原理,将 NO2、O2和熔融 KNO3制成燃料电池,其原理如图,该电池在工作过程中NO2转变成绿色硝化剂Y,Y是一种氧化物,可循环使用,石墨Ⅰ附近发生的反应电极反应式为_____相同条件下,消耗的 O2和 NO2的体积比为_____