题目内容
【题目】对于可逆反应 N2(g)+3H2(g)2NH3(g) △H<0,下列研究目的和图示相符的是
A.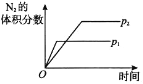 压强对反应的影响(p2>p1)
压强对反应的影响(p2>p1)
B.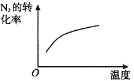 温度对反应的影响
温度对反应的影响
C.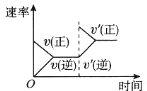 平衡体系增加 N2对反应的影响
平衡体系增加 N2对反应的影响
D.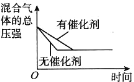 催化剂对反应的影响
催化剂对反应的影响
【答案】C
【解析】
A.增大压强,合成氨的化学反应速率加快,化学平衡正向移动,根据图示知道压强应该是p2<p1,且P1条件下,氨气的百分含量更大,故A错误;
B.升高温度,化学反应向着逆反应方向进行,反应物氮气转化率减小,故B错误;
C.增加反应物的浓度,化学平衡向着正反应方向移动,正反应速率大于逆反应速率,故C正确;
D.加入催化剂可以加快化反应速率,应该是缩短达平衡的时间,但是不会引起平衡的移动,故D错误;
故答案为C。

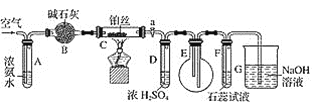
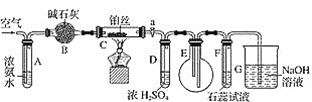
【题目】科学家研究出一种以天然气为燃料的“燃烧前捕获系统”,其简单流程如图所示(条件及物质未标出)。

(1)已知:CH4、CO、H2的燃烧热分别为890.3 kJ·mol-1、283.0 kJ·mol-1、285.8 kJ·mol-1,则上述流程中第一步反应2CH4(g)+O2(g)===2CO(g)+4H2(g)的ΔH=______________。
(2)工业上可用H2和CO2制备甲醇,其反应方程式为CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g),某温度下,将1 mol CO2和3 mol H2充入体积不变的2 L密闭容器中,发生上述反应,测得不同时刻反应前后的压强关系如下表:
CH3OH(g)+H2O(g),某温度下,将1 mol CO2和3 mol H2充入体积不变的2 L密闭容器中,发生上述反应,测得不同时刻反应前后的压强关系如下表:
时间/h | 1 | 2 | 3 | 4 | 5 | 6 |
| 0.90 | 0.85 | 0.83 | 0.81 | 0.80 | 0.80 |
①用H2表示前2 h 的平均反应速率v(H2)=_________________________________;
②该温度下,CO2的平衡转化率为________。
(3)在300 ℃、8 MPa下,将CO2和H2按物质的量之比1∶3 通入一密闭容器中发生(2)中反应,达到平衡时,测得CO2的平衡转化率为50%,则该反应条件下的平衡常数为Kp=________(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(4)CO2经催化加氢可合成低碳烯烃:2CO2(g)+6H2(g)![]() C2H4(g)+4H2O(g) ΔH。在0.1 MPa时,按n(CO2)∶n(H2)=1∶3投料,如图所示为不同温度(T)下,平衡时四种气态物质的物质的量(n)关系。
C2H4(g)+4H2O(g) ΔH。在0.1 MPa时,按n(CO2)∶n(H2)=1∶3投料,如图所示为不同温度(T)下,平衡时四种气态物质的物质的量(n)关系。

①该反应的ΔH________0(填“>”或“<”)。
②曲线c表示的物质为_______。
③为提高H2的平衡转化率,除改变温度外,还可采取的措施______________。(答出一条即可)