题目内容
14.下列化合物中,含有极性共价键的离子化合物是( )| A. | Ca(OH)2 | B. | N2H4 | C. | Na2S2 | D. | NH4NO3 |
分析 活泼金属和活泼非金属元素之间易形成离子键,同种非金属元素之间易形成极性键,不同非金属元素之间易形成极性键,含有离子键的化合物是离子化合物,据此分析解答.
解答 解:A.氢氧化钙中钙离子和氢氧根离子之间存在离子键,氢氧根离子中H-O原子之间存在极性键,为离子化合物,故A正确;
B.肼中N-N原子之间存在非极性键,N-H原子之间存在极性键,为共价化合物,故B错误;
C.Na2S2中钠离子和S22-中存在离子键,S22-中存在S-S非极性键,为离子化合物,故C错误;
D.硝酸铵中铵根离子和硝酸根离子之间存在离子键,铵根离子中N-H原子之间存在极性键、硝酸根离子中N-O原子之间存在极性键,为离子化合物,故D正确;
故选AD.
点评 本题考查化学键判断,侧重考查基本概念,明确物质构成微粒及微粒之间作用力即可解答,注意铵盐属于离子化合物,但不含金属元素.

练习册系列答案
 金博士一点全通系列答案
金博士一点全通系列答案
相关题目
4.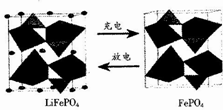 LiFePO4是锂离子电池一种电极材料,其结构稳定、资源丰富、安全性能好、无毒.该电极材料在充放电时的变化如图所示,下列有关说法正确的是( )
LiFePO4是锂离子电池一种电极材料,其结构稳定、资源丰富、安全性能好、无毒.该电极材料在充放电时的变化如图所示,下列有关说法正确的是( )
 LiFePO4是锂离子电池一种电极材料,其结构稳定、资源丰富、安全性能好、无毒.该电极材料在充放电时的变化如图所示,下列有关说法正确的是( )
LiFePO4是锂离子电池一种电极材料,其结构稳定、资源丰富、安全性能好、无毒.该电极材料在充放电时的变化如图所示,下列有关说法正确的是( )| A. | 放电时该电极为负极 | |
| B. | 充电是Li+向阳极移动 | |
| C. | 充电时该电极发生氧化反应,反应式为LiFePO4-e-=FePO4+Li+ | |
| D. | 该电池可以用磷酸溶液作电解质 |
5.下列有关物质性质与应用对应关系错误的是( )
| A. | 常温下,浓硫酸能使铝钝化,可用铝制容器贮运浓硫酸 | |
| B. | 二氧化硅熔点很高、硬度很大,可用于制造坩埚 | |
| C. | 氯化铁溶液能腐蚀铜,可用于制作印刷电路板 | |
| D. | 金属钠硬度小、密度小,可用于制造高压钠灯 |
9.下表所示的五种元素中,W、X、Y、Z为短周期元素,X元素的单质是空气中含量最多的成分.下列说法正确的是( )
| X | Y | ||
| W | Z | ||
| T |
| A. | X位于元素周期表中第二周期ⅤA族 | |
| B. | Y、Z形成氢化物的沸点更高是Z | |
| C. | 由X、Y和氢三种元素形成的化合物中只有共价键 | |
| D. | 元素T与X的原子序数相差25 |
19.固体粉末X中可能含有FeO、Fe2O3、MnO2、K2SiO3、K2SO3、KAlO2、MgCl2、K2CO3、NaNO2中的若干种.为确定该固体粉末的成分,现取X进行连续实验,实验过程及产物如下:(注:亚硝酸:中强酸,既具有氧化性又具有还原性,不很稳定,在水溶液中易发生岐化反应.)

根据上述实验,以下说法正确的是( )

根据上述实验,以下说法正确的是( )
| A. | 溶液甲中一定含有K2SiO3、NaNO2,可能含有KAlO2、K2CO3 | |
| B. | 由于在溶液甲中加入足量稀盐酸后再加入BaCl2溶液,因此无法判断溶液中是否有K2SO3 | |
| C. | 气体A和气体D一定均为纯净物 | |
| D. | 原混合物中一定含有MnO2、Fe2O3 |
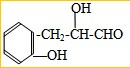
6.有关如图所示的有机物的说法不正确的是( )
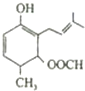

| A. | 该有机物可以与NaOH溶液反应 | |
| B. | 该有机物的分子式为C13H19O3 | |
| C. | 该有机物既可以发生氧化反应又能发生还原反应 | |
| D. | 该有机物和丙三醇不互为同系物 |
3.现有7瓶失去了标签的液体,已知它们是有机溶剂,可能是①乙醇②乙酸 ③苯④乙酸乙酯 ⑤油脂⑥葡萄糖⑦蔗糖溶液,现通过如下实验步骤来确定试剂中所装的液体名称.
(1)试给它们的试剂瓶重新贴上标签:
A乙醇、B乙酸、C苯、D乙酸乙酯、E油脂、F葡萄糖溶液、G蔗糖溶液;
(2)写出在D中加入NaOH溶液并加热的化学方程式.CH3COOCH2CH3+NaOH$\stackrel{△}{→}$CH3COONa+CH3CH2OH
(3)已知乙醛发生银镜反应的化学方程式为:
CH3CHO+4[Ag(NH3)2]OH $\stackrel{△}{→}$ (NH4)2CO3+4Ag↓+6NH3↑+2H2O.
试写出葡萄糖发生银镜反应的化学方程式为CH2OH(CHOH)4CHO+2Ag(NH3)2OH$\stackrel{△}{→}$H2O+2Ag↓+3NH3+CH2OH(CHOH)4COONH4.
| 实验步骤和方法 | 实验现象 |
| ①把7瓶液体分别依次标号A、B、C、D、E、F、G后闻气味 | 只有F、G两种液体没有气味 |
| ②各取少量于试管中加水稀释 | 只有C、D、E三种液体不溶解而浮在水上层 |
| 分别取少量7种液体于试管中加新制的Cu(OH)2并加热 | 只有B使沉淀溶解,F中产生红色沉淀 |
| 各取C、D、E少量于试管中,加稀NaOH溶液并加热 | 只有C仍有分层现象,且在D的试管中闻到特殊香味 |
A乙醇、B乙酸、C苯、D乙酸乙酯、E油脂、F葡萄糖溶液、G蔗糖溶液;
(2)写出在D中加入NaOH溶液并加热的化学方程式.CH3COOCH2CH3+NaOH$\stackrel{△}{→}$CH3COONa+CH3CH2OH
(3)已知乙醛发生银镜反应的化学方程式为:
CH3CHO+4[Ag(NH3)2]OH $\stackrel{△}{→}$ (NH4)2CO3+4Ag↓+6NH3↑+2H2O.
试写出葡萄糖发生银镜反应的化学方程式为CH2OH(CHOH)4CHO+2Ag(NH3)2OH$\stackrel{△}{→}$H2O+2Ag↓+3NH3+CH2OH(CHOH)4COONH4.
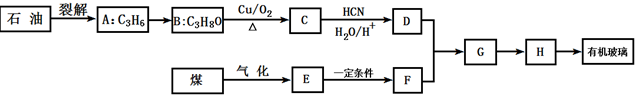
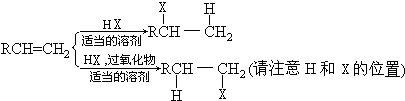
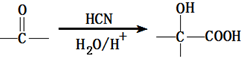
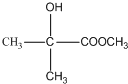 ;有机玻璃的链节是:
;有机玻璃的链节是: ;
;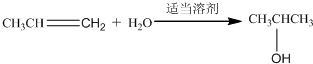 ;
;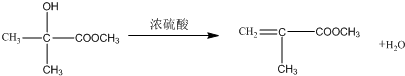 .
.
 ;
; 或
或 .
.