题目内容
3.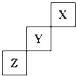 短周期元素X、Y、Z在周期表中位置关系如图所示,
短周期元素X、Y、Z在周期表中位置关系如图所示,(1)X元素的名称是氦.
(2)Y在元素周期表中的位置是第二周期第VIIA族,它形成单质的化学式是F2.
(3)Z元素的原子结构示意图为
 .写出Z单质与铁反应的化学反应方程式:Fe+S$\frac{\underline{\;\;△\;\;}}{\;}$FeS.
.写出Z单质与铁反应的化学反应方程式:Fe+S$\frac{\underline{\;\;△\;\;}}{\;}$FeS.
分析 X、Y、Z属于短周期元素,根据元素在周期表中的位置知,X是He元素、Y是F元素、Z是S元素,S的氧化性较弱,与铁反应生成FeS,以此解答该题.
解答 解:X、Y、Z属于短周期元素,根据元素在周期表中的位置知,X是He元素、Y是F元素、Z是S元素,
(1)由X在周期表中的位置可知X为氦,故答案为:氦;
(2)Y为F,位于周期表第二周期第VIIA族,形成的单质为F2,故答案为:第二周期第VIIA族;F2;
(3)Z为S,原子核外有3个电子层,最外层电子数为6,原子结构示意图为 ,与铁反应生成FeS,方程式为Fe+S$\frac{\underline{\;\;△\;\;}}{\;}$FeS,
,与铁反应生成FeS,方程式为Fe+S$\frac{\underline{\;\;△\;\;}}{\;}$FeS,
故答案为: ;Fe+S$\frac{\underline{\;\;△\;\;}}{\;}$FeS.
;Fe+S$\frac{\underline{\;\;△\;\;}}{\;}$FeS.
点评 本题考查元素周期表、原子结构、性质的关系应用,为高频考点,侧重于学生的分析能力的考查,难度不大,推断元素是解题关键,注意对基础知识的理解掌握.

练习册系列答案
相关题目
13.实验探究:为了研究同周期元素性质递变规律,某同学自己设计了一套实验方案,并动手记录实验步骤和现象如下:(表中的“实验步骤”与“实验现象”前后不一定是对应关系)
请你帮助该同学整理并完成实验报告:
(1)实验用品:试剂:金属钠、镁条、铝条、稀盐酸、AlC13溶液、NaOH溶液、酚酞溶液等.
实验所用到的玻璃仪器:①试管、②烧杯、③酒精灯以及胶头滴管、玻璃片等.
(2)实验内容:(填写与实验步骤对应的实验现象的编号和②的化学方程式)
(3)此实验的结论:钠、镁、铝的金属性强弱Na>Mg>Al.
| 实验步骤 | 实验现象 |
| ①将镁条用砂纸打磨后,放入试管中,加入少量水后,加热至水沸腾;再向溶液中滴加酚酞溶液 | A.浮在水面上,熔成小球,四处游动,发出“嘶嘶”声,随之消失,溶液变成红色. |
| ②在盛有冷水的烧杯中滴入几滴酚酞溶液,再将一小块金属钠放入其中 | B.有气体产生,溶液变成浅红色 |
| ③将镁条投入稀盐酸中 | C.剧烈反应,迅速产生大量无色气体 |
| ④将铝条投入稀盐酸中 | D.反应不十分剧烈;产生无色气体. |
| ⑤向A1Cl3溶液中滴加NaOH溶液至过量 | E.生成白色胶状沉淀,继而沉淀消失 |
(1)实验用品:试剂:金属钠、镁条、铝条、稀盐酸、AlC13溶液、NaOH溶液、酚酞溶液等.
实验所用到的玻璃仪器:①试管、②烧杯、③酒精灯以及胶头滴管、玻璃片等.
(2)实验内容:(填写与实验步骤对应的实验现象的编号和②的化学方程式)
| 实验内容 | ① | ② | ③ | ④ | ⑤ |
| 实验现象(填A~F) | B |
14.NA为阿伏加德罗常数,下列说法正确的是( )
| A. | 标准状况下,11.2 L的丙烷所含的氢原子数为4NA | |
| B. | 16g甲烷所含电子数目为16NA | |
| C. | 标准状况下,11.2 L三氯甲烷所含分子数为0.5NA | |
| D. | 14 g乙烯的原子数为3NA |
11.在铜锌原电池中,锌电极上发生的反应为Zn-2e-=Zn2+,则不正确的是( )
| A. | 锌电极为负极 | B. | 铜电极为正极 | C. | 反应中Zn被氧化 | D. | 反应中铜被还原 |
18.在制造玻璃和水泥都用到的原料是( )
| A. | 石灰石 | B. | 纯碱 | C. | 黏土 | D. | 石英 |
8.关于SO2和Cl2的叙述错误的是( )
| A. | 都是大气污染物 | B. | 都可以用碱石灰干燥 | ||
| C. | 都能给NaOH溶液吸收 | D. | 都可以用向上排空气法收集 |
12.下列分子中所有碳原子肯定在同一平面上的是( )
| A. | 丁烷 | B. | 异丁烷 | C. | CH3CH=CHCH3 | D. | CH2=CHCH2CH3 |
13.下列说法正确的是( )
| A. | 可通过热还原法制备金属铝和铁 | |
| B. | 工业制硫酸产生的废气需用石灰水吸收 | |
| C. | 淀粉、植物油、蛋白酶均为高分子化合物 | |
| D. | 水晶、玛瑙、光导纤维、陶瓷的主要成分都是二氧化硅 |
 ,故它在周期表的位置是第三周期第ⅥA族,它对应形成的阴离子结构示意图为
,故它在周期表的位置是第三周期第ⅥA族,它对应形成的阴离子结构示意图为 .该元素的最高正化合价为+6,最低负化合价为-2.
.该元素的最高正化合价为+6,最低负化合价为-2.