题目内容
13.下列说法正确的是( )| A. | 可通过热还原法制备金属铝和铁 | |
| B. | 工业制硫酸产生的废气需用石灰水吸收 | |
| C. | 淀粉、植物油、蛋白酶均为高分子化合物 | |
| D. | 水晶、玛瑙、光导纤维、陶瓷的主要成分都是二氧化硅 |
分析 A.铝性质活泼;
B.制硫酸产生的废气是酸性气体;
C.油脂不是高分子化合物;
D.陶瓷的主要成分是硅酸盐.
解答 解:A.铝性质活泼应用电解法冶炼,故A错误;
B.制硫酸产生的废气是酸性气体,可用石灰水吸收,故B正确;
C.油脂相对分子质量较小,不是高分子化合物,故C错误;
D.陶瓷的主要成分是硅酸盐,不是二氧化硅,故D错误.
故选B.
点评 本题考查金属冶炼、尾气吸收、高分子化合物和硅酸盐等,难度较小,旨在考查学生对基础知识的识记,注意基础知识的积累掌握.

练习册系列答案
 发散思维新课堂系列答案
发散思维新课堂系列答案
相关题目
3.在容积固定的密闭容器中通入各为1mol的A、C、D和n mol B,发生如下反应A(g)+4B(g)?C(g)+2D(g).当n在一定范围内变化时,均可通过调节反应器的温度,使反应达到平衡时保持容器中气体总物质的量为5mol,若使起始反应向正反应方向进行,则n的取值范围是( )
| A. | 1<n<2 | B. | 1<n<5 | C. | 2<n<4 | D. | 2<n<5 |
7.某市大气质量监测站对市区出现雾霾时的大气监测发现:首先要污染物为PM2.5,并对其进行分析.
(1)将PM2.5样本用蒸馏水处理制成待测试样.若测得该试样所含水溶性无机离子的化学组分及浓度如下表:
根据表中数据计算该试样的pH=5.
(2)该地区若有降雨则可大大缓解雾霾天气,但也会带来另一种环境问题:形成酸雨.
(3)环境治理要从根源一着手,减少SO2、NO2等气体的排放是重要措施.汽车发动机工作时气缸中会引发N2和O2的反应,其能时变化示意图如下:
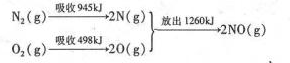
①写出该反应的热化学方程式:N2(g)+O2(g)=2NO(g)△H=+184kJ•mol-1.
②汽车启动后,气缸温度越高,单位时间内NO的排放量越大,其原因是:正反应为吸热反应,升高温度,平衡向着正向移动.
③将NO2变成无害的N2要找到合适的物质G与适当的反应条件,G应为还原剂(填“还原剂”或“氧化剂”).下式中X必须为无污染的物质,化学计量数n可为0.NO2+G→N2+H2O+nX(未配平的反应式)
下列化合物中满足上述反反应式式中的G是ad(填字母代号).
a.NH3 b.CO2 c.SO2 d.CH3CH2OH
(4)利用电化学传感器能够准确、快速地测定NO2的含量.一种以ZrO2为固体电解质(传递O2-),总反应为:2NO+O2=2NO2,则其负极的电极反应为NO+O2--2e-=NO2.若传感器检测的电子流量为1×10-3mol/s,则通过传感器的NO的流量为15mg/s.
(1)将PM2.5样本用蒸馏水处理制成待测试样.若测得该试样所含水溶性无机离子的化学组分及浓度如下表:
| 离子 | Ca2+ | Na+ | NH4+ | SO42- | NO3- | Cl- |
| 浓度/mol.L-1 | 2×10-6 | 6×10-6 | 2×10-5 | 4×10-6 | 3×10-5 | 2×10-6 |
(2)该地区若有降雨则可大大缓解雾霾天气,但也会带来另一种环境问题:形成酸雨.
(3)环境治理要从根源一着手,减少SO2、NO2等气体的排放是重要措施.汽车发动机工作时气缸中会引发N2和O2的反应,其能时变化示意图如下:

①写出该反应的热化学方程式:N2(g)+O2(g)=2NO(g)△H=+184kJ•mol-1.
②汽车启动后,气缸温度越高,单位时间内NO的排放量越大,其原因是:正反应为吸热反应,升高温度,平衡向着正向移动.
③将NO2变成无害的N2要找到合适的物质G与适当的反应条件,G应为还原剂(填“还原剂”或“氧化剂”).下式中X必须为无污染的物质,化学计量数n可为0.NO2+G→N2+H2O+nX(未配平的反应式)
下列化合物中满足上述反反应式式中的G是ad(填字母代号).
a.NH3 b.CO2 c.SO2 d.CH3CH2OH
(4)利用电化学传感器能够准确、快速地测定NO2的含量.一种以ZrO2为固体电解质(传递O2-),总反应为:2NO+O2=2NO2,则其负极的电极反应为NO+O2--2e-=NO2.若传感器检测的电子流量为1×10-3mol/s,则通过传感器的NO的流量为15mg/s.
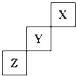 短周期元素X、Y、Z在周期表中位置关系如图所示,
短周期元素X、Y、Z在周期表中位置关系如图所示, .写出Z单质与铁反应的化学反应方程式:Fe+S$\frac{\underline{\;\;△\;\;}}{\;}$FeS.
.写出Z单质与铁反应的化学反应方程式:Fe+S$\frac{\underline{\;\;△\;\;}}{\;}$FeS. 在一定条件下,N2(g)+H2(g)?2NH3(g),该反应的能量变化为放出92.4KJ热量,在容积为2升的密闭容器中,分别充入1molN2和1molH2,2min反应达到最大限度,三种气态物质的量随时间的变化曲线如图所示.根据图中数据,试填写下列空白:
在一定条件下,N2(g)+H2(g)?2NH3(g),该反应的能量变化为放出92.4KJ热量,在容积为2升的密闭容器中,分别充入1molN2和1molH2,2min反应达到最大限度,三种气态物质的量随时间的变化曲线如图所示.根据图中数据,试填写下列空白: ,
, .
.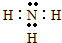 ,
,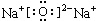 (或
(或 ).
).