题目内容
水热法制备Fe3O4纳米颗粒的总反应:3Fe2++2S2O32-+O2+xOH- Fe3O4+S4O62-+2H2O,有关说法正确的是
Fe3O4+S4O62-+2H2O,有关说法正确的是
 Fe3O4+S4O62-+2H2O,有关说法正确的是
Fe3O4+S4O62-+2H2O,有关说法正确的是| A.每转移1.5mol电子,有1.125mol Fe2+被氧化 |
| B.x = 2 |
| C.Fe2+、S2O32-都是还原剂 |
| D.每生成1mol Fe3O4,转移电子2mol |
C
试题分析:在3Fe2++2 S2O32﹣+O2+xOH﹣=Fe3O4+S4O62﹣+2H2O中,化合物中铁元素、硫元素用平均化合价,铁元素的化合价变化:+2→+
 ;硫元素的化合价变化为:+2→+
;硫元素的化合价变化为:+2→+ ;氧元素的化合价变化:0→﹣2,所以氧化剂是O2还原剂是Fe2+、S2O32﹣,还原产物是Fe3O4,设失电子xmol,由3Fe2+﹣﹣Fe3O4﹣失2e﹣,1molFe2+被氧化时失去的电子为
;氧元素的化合价变化:0→﹣2,所以氧化剂是O2还原剂是Fe2+、S2O32﹣,还原产物是Fe3O4,设失电子xmol,由3Fe2+﹣﹣Fe3O4﹣失2e﹣,1molFe2+被氧化时失去的电子为 mol,根据氢原子守恒,水的化学计量数为2,则OH﹣的化学计量数为4,即x=4。3O4是复杂的化合物,铁元素既有+2价也有+3价,把Fe3O4中铁元素的化合价用平均化合价处理,S2O32﹣的硫元素的化合价用平均化合价处理是解本题的关键,本题难度较大,需细心分析。
mol,根据氢原子守恒,水的化学计量数为2,则OH﹣的化学计量数为4,即x=4。3O4是复杂的化合物,铁元素既有+2价也有+3价,把Fe3O4中铁元素的化合价用平均化合价处理,S2O32﹣的硫元素的化合价用平均化合价处理是解本题的关键,本题难度较大,需细心分析。
练习册系列答案
 全能测控期末小状元系列答案
全能测控期末小状元系列答案
相关题目

 。
。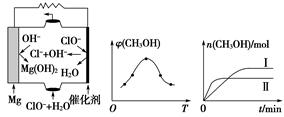
 CH3OH(g)+H2O(g) ΔH。
CH3OH(g)+H2O(g) ΔH。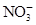 、Fe3+、
、Fe3+、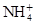 、H2O和H+六种粒子,分别属于同一氧化还原反应中的反应物和生成物,下列叙述错误的是( )
、H2O和H+六种粒子,分别属于同一氧化还原反应中的反应物和生成物,下列叙述错误的是( )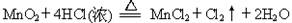
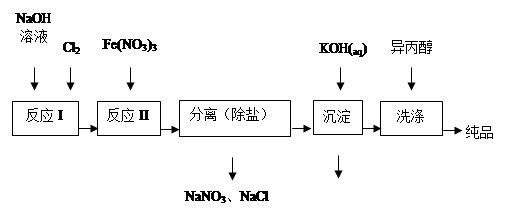 ①洗涤粗品时选用异丙醇而不用水的理由是: 。
①洗涤粗品时选用异丙醇而不用水的理由是: 。 6Cu+SO2,该反应的氧化剂是___________________;当生成19.2gCu时,反应中转移的电子为____________mol。
6Cu+SO2,该反应的氧化剂是___________________;当生成19.2gCu时,反应中转移的电子为____________mol。