题目内容
有4.8g CuO、Fe2O3混合物跟足量CO充分反应后固体减少1.28g,反应后全部气体用0.6mol/L Ba(OH)2溶液100mL吸收。下列有关叙述中正确的是
| A.原混合物中CuO与Fe2O3物质的量的比为l:l |
| B.原混合物中CuO与Fe2O3的质量比为2:1 |
| C.吸收CO2后的溶液中一定有Ba(HCO3)2 |
| D.吸收CO2后的溶液中生成白色沉淀的质量为11.82 g |
AC
解析试题分析:A、CuO、Fe2O3混合物跟足量CO充分反应,固体减少质量为混合物中含有的氧元素的质量,混合物中氧原子的物质的量为1.28g÷16g/mol=0.08mol。设混合物中CuO、Fe2O3的物质的量分别为xmol、ymol,则:x+3y=0.08、80x+160y=4.8,解得x=0.02、y=0.02,故原混合物中CuO与Fe2O3物质的量的比为0.02mol:0.02mol=l:l,故A正确;B、原混合物中CuO、Fe2O3的质量之比为80g/mol×0.02mol:160g/mol×0.02mol=1:2,故B错误;C、CO获得1个O原子生成CO2,故n(CO2)=n(O)=0.08mol,n[Ba (OH)2]=0.6mol/L×0.1L=0.06mol,故n(CO2):n[Ba (OH)2]=0.08mol:0.06mol=4:3,介于1:1与2:1之间,故生成碳酸钡与碳酸氢钡,因此选项C正确;D、令碳酸钡与碳酸氢钡物质的量分别为amol、bmol,根据钡离子守恒、碳元素守恒可知a+2b=0.08、a+b=0.6×0.1,解得a=0.04,b=0.02,故生成碳酸钡的质量为0.04mol×197g/mol=7.88g,因此D错误,答案选AC。
考点:考查混合物计算的有关正误判断

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案将35.8g Al、Fe、Cu组成的合金溶于足量的NaOH溶液中,产生6.72L气体(标准状况)。另取等质量的该合金溶于过量的稀硝酸中,生成13.44L NO(标准状况),向反应后的溶液中加入足量的NaOH溶液,得到沉淀的质量为
| A.66.4 g | B.50.8 g | C.44.8g | D.39.2g |
若NA表示阿伏加德罗常数的值,下列说法正确的是
| A.铁制品上电镀锌时,阴极质量每增加65g时转移的电子数是2NA |
| B.5.6L Cl2与足量铁粉反应时转移的电子数为0.5NA |
| C.1L 1mol·L-1的CH3COOH溶液中含有H+的数目是NA |
| D.1L 0.5mol·L-1的Na2CO3溶液中含有CO32-的数目是0.5NA |
用NA表示阿伏加德罗常数的值。下列叙述中正确的是
| A.1mol SiO2中含有NA个SiO2分子 |
| B.1mol Cu与足量的稀HNO3反应,转移2 NA个电子 |
| C.1 L0.1mol . L-1Na2CO3溶液中含有 0.1NA个CO32- |
| D.1mol苯乙烯中含有的碳碳双键数为4NA |
有关物质结构的表述错误的是
| A.氯乙烯的结构简式:CH2="CHCl" |
B.氮分子的结构式: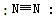 |
| C.氨分子的空间构型:三角锥形 |
| D.氯离子的最外层电子排布式:3s23p6 |
将3.52 g CO2和SO2混合气体通入一定量的NaOH溶液中,气体全部与NaOH反应生成盐,将反应后的溶液减压低温蒸干后得到不含结晶水的固体,固体的质量可能为
| A.8.48 g | B.7.48 g | C.5.72 g | D.5.22g |
如图是某学校实验室从化学试剂商店买回的硫酸试剂标签上的部分内容。 据此下列说法错误的是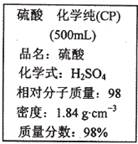
| A.该硫酸具有强烈的腐蚀性,应放于危险化学用品柜中妥善保管 |
| B.取10 mL该硫酸于烧杯中,再加等体积的水,可配得49%的硫酸 |
| C.配制200mL4.6 mol·L-1的稀硫酸需取该硫酸50 mL |
| D.该硫酸与等质量的水混合所得溶液的物质的量浓度小于9.2 mol·L-1 |
下列化学用语不正确的是
A.二氧化碳的电子式是: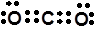 |
B.铝离子的结构示意图是: 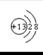 |
C. 的中子数与质子数之差是2 的中子数与质子数之差是2 |
| D.Na2O2中的阳离子数与阴离子数之比为1:1 |
设NA表示阿伏加德罗常数的值,下列说法正确的是
| A.常温常压下,5.6L CH4含C—H键数目为NA |
| B.常温常压下,100g17%H2O2水溶液含氧原子总数为NA |
| C.标准状况下,5.6L O2与适量Na加热反应,转移电子数一定为NA |
| D.常温常压下,14g乙烯与丙烯的混合气体,含碳原子总数为NA |