题目内容
8.某有机物具有下列性质:能发生银镜反应;滴入石蕊试液不变色;加入少量碱液并滴入酚酞试液,共煮时红色逐渐消失.该有机物可能是( )| A. | 甲酸乙酯 | B. | 甲酸 | C. | 乙酸 | D. | 乙酸甲酯 |
分析 能发生银镜反应说明含有醛基,滴入紫色石蕊试液不变色,说明不含羧基;滴入少量碱液并滴入酚酞试液共煮后,红色消失,则该物质水解生成羧酸钠,说明含有酯基,据此分析解答.
解答 解:A、甲酸乙酯中含有醛基,能发生银镜反应,不含羧基,所以不能使紫色石蕊试液变色,含有酯基能水解,所以符合条件,故A正确;
B、甲酸中含有醛基和羧基,能发生银镜反应也能使紫色石蕊试液变色,不符合条件,故B错误;
C、乙酸中不含有醛基,故C错误;
D、乙酸甲酯中不含醛基,所以不能发生银镜反应,不符合条件,故D错误,故选A.
点评 本题考查有机物结构和性质,为高频考点,明确官能团及其性质关系是解本题关键,注意能发生银镜反应的不一定是醛,可能是甲酸或甲酸某酯,为易错点.

练习册系列答案
 备战中考寒假系列答案
备战中考寒假系列答案
相关题目
18.甲醇质子交换膜燃料电池中将甲醇蒸气转化为氢气的两种反应原理是:
①CH3OH(g)+H2O(g)═CO2(g)+3H2(g)△H=+49.0kJ•mol-1
②CH3OH(g)+$\frac{1}{2}$O2(g)═CO2(g)+2H2(g)△H=-192.9kJ•mol-1
下列说法正确的是( )
①CH3OH(g)+H2O(g)═CO2(g)+3H2(g)△H=+49.0kJ•mol-1
②CH3OH(g)+$\frac{1}{2}$O2(g)═CO2(g)+2H2(g)△H=-192.9kJ•mol-1
下列说法正确的是( )
| A. | CH3OH的燃烧热为192.9 kJ•mol-1 | |
| B. | 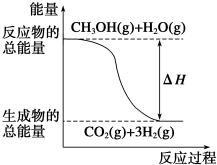 反应①中的能量变化如图所示 | |
| C. | CH3OH转变成H2的过程一定要吸收能量 | |
| D. | 根据②推知反应CH3OH(l)+$\frac{1}{2}$O2(g)═CO2(g)+2H2(g)的△H>-192.9 kJ•mol-1 |
19.下列实验操作与实验目的相对应的是( )
| A. | 实验操作:制乙炔用饱和食盐水代替水,实验目的:加快化学反应速率 | |
| B. | 实验操作:C2H4与SO2混合气体通过盛有溴水的洗气瓶,实验目的:除去C2H4中的SO2 | |
| C. | 实验操作:淀粉溶液水解后冷却至温室,加碘水观察现象,实验目的:检验淀粉是否水解完全 | |
| D. | 实验操作:将溴乙烷与氢氧化钠水溶液共热一段时间,再向冷却后的混合液中滴加硝酸银溶液,实验目的:检验溴乙烷中的溴原子 |
16.常温下,下列水溶液pH<7的是( )
| A. | Na2CO3 | B. | NH4Cl | C. | NaCl | D. | Na2SO4 |
3.稀土元素是指元素周期表中原子序数为57到71的15种镧系元素,以及与镧系元素化学性质相似的钪(Sc)和钇(Y)共17 种元素.稀土有“工业维生素”的美称,如今已成为极其重要的战略资源.
几种稀土元素的电离能(单位:kJ•mol-1)
(1)离子化合物 Na3[Sc(OH)6]中,存在的作用力除离子键外还有共价键和配位键.
(2)Sm(钐)的单质与1,2-二碘乙烷可发生如下反应:Sm+ICH2CH2I→SmI2+CH2=CH2.
ICH2CH2I中碳原子杂化轨道类型为sp3,1mol CH2=CH2中含有的σ键数目为5NA.常温下1,2-二碘乙烷为液体而乙烷为气体,其主要原因是二碘乙烷的相对分子质量较大,分子间作用力较强,沸点相对较高.
(3)PrO2(二氧化镨)的晶体结构与CaF2相似,晶胞中Pr(镨)原子位于面心和顶点.则PrO2(二氧化镨)的晶胞中有8个氧原子.
(4)Ce(铈)单质为面心立方晶体,其胞参数为a=516pm.晶胞中Ce(铈)原子的配位数为12,列式表示Ce(铈)单质的密度:$\frac{4×140}{6.02×1{0}^{23}×({516×1{0}^{-10})}^{3}}$g•cm-3(不必计算出结果).
几种稀土元素的电离能(单位:kJ•mol-1)
| 元素 | I1 | I2 | I3 | I1+I2+I3 | I4 |
| Sc(钪) | 633 | 1235 | 2389 | 4257 | 7019 |
| Y(钇) | 616 | 1181 | 1980 | 3777 | 5963 |
| La(镧) | 538 | 1067 | 1850 | 3455 | 4819 |
| Ce(铈) | 527 | 1047 | 1949 | 3523 | 3547 |
(2)Sm(钐)的单质与1,2-二碘乙烷可发生如下反应:Sm+ICH2CH2I→SmI2+CH2=CH2.
ICH2CH2I中碳原子杂化轨道类型为sp3,1mol CH2=CH2中含有的σ键数目为5NA.常温下1,2-二碘乙烷为液体而乙烷为气体,其主要原因是二碘乙烷的相对分子质量较大,分子间作用力较强,沸点相对较高.
(3)PrO2(二氧化镨)的晶体结构与CaF2相似,晶胞中Pr(镨)原子位于面心和顶点.则PrO2(二氧化镨)的晶胞中有8个氧原子.
(4)Ce(铈)单质为面心立方晶体,其胞参数为a=516pm.晶胞中Ce(铈)原子的配位数为12,列式表示Ce(铈)单质的密度:$\frac{4×140}{6.02×1{0}^{23}×({516×1{0}^{-10})}^{3}}$g•cm-3(不必计算出结果).
13.下列各组物质的性质比较,正确的是( )
| A. | 还原性:F-<Cl-<Br-<I- | B. | 碱性:NaOH<Mg(OH)2<Al(OH)3 | ||
| C. | 氢化物稳定性:H2S>HF>H2O | D. | 酸性:HClO4>H3PO4>H2SO4 |
20.可以鉴别乙酸溶液、葡萄糖溶液、乙醇溶液的试剂是( )
| A. | NaOH溶液 | B. | 新制氢氧化铜悬浊液 | ||
| C. | 石蕊试液 | D. | 碳酸钠溶液 |
17.已知短周期元素的离子 aA2+、bB+、cC3-、dD-都具有相同的电子层结构,则下列叙述正确的是( )
| A. | 原子序数 d>c>b>a | B. | 原子半径 A>B>D>C | ||
| C. | 离子半径 C>D>B>A | D. | 单质的还原性 A>B>D>C |
18. “茶倍健”牙膏中含有茶多酚,但茶多酚是目前尚不能人工合成的纯天然、多功能、高效能的抗氧化剂和自由基净化剂.其中没食子儿茶素(EGC)的结构如图所示.关于EGC的下列叙述中正确的是( )
“茶倍健”牙膏中含有茶多酚,但茶多酚是目前尚不能人工合成的纯天然、多功能、高效能的抗氧化剂和自由基净化剂.其中没食子儿茶素(EGC)的结构如图所示.关于EGC的下列叙述中正确的是( )
 “茶倍健”牙膏中含有茶多酚,但茶多酚是目前尚不能人工合成的纯天然、多功能、高效能的抗氧化剂和自由基净化剂.其中没食子儿茶素(EGC)的结构如图所示.关于EGC的下列叙述中正确的是( )
“茶倍健”牙膏中含有茶多酚,但茶多酚是目前尚不能人工合成的纯天然、多功能、高效能的抗氧化剂和自由基净化剂.其中没食子儿茶素(EGC)的结构如图所示.关于EGC的下列叙述中正确的是( )| A. | 分子中所有的原子共面 | B. | 1molEGC与3molNaOH恰好完全反应 | ||
| C. | 它具有酯的性质 | D. | 遇FeCl3溶液发生显色反应 |