题目内容
【题目】铜及其化合物在工农业生产及日常生活中应用非常广泛.
(1)由辉铜矿制取铜的反应过程为:
2Cu2S(s)+3O2 (g)=2Cu2O(s)+2SO2(g)△H=﹣768.2kJmol﹣1 ,
2Cu2O(s)+Cu2S(s)=6Cu(s)+SO2(g)△H=+116.0kJmol﹣1 ,
请写出Cu2S与O2反应生成Cu与SO2的热反应方程式: .
(2)氯化铜溶液中铜各物种的分布分数(平衡时某物种的浓度占各物种浓度之和的分数)与c(Cl﹣) 的关系如图1.①当c(Cl﹣)=9molL﹣1时,溶液中主要的3种含铜物种浓度大小关系为 . 
②在c(Cl﹣)=1molL﹣1的氯化铜溶液中,滴入AgNO3溶液,含铜物种间转化的离子方程式为(任写一个).
(3)电解Na2HPO3溶液可得到亚磷酸,装置如图2
(说明:阳膜只允许阳离子通过,阴膜只允许阴离子通过)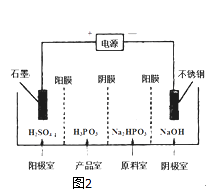
①阳极的电极反应式为: .
②产品室中反应的离子方程式为: .
【答案】
(1)Cu2S(s)+O2(g)═2Cu(s)+SO2(g)△H=﹣217.4KJ/mol
(2)c(CuCl2)>c(CuCl+)>c(CuCl3﹣);CuCl+═Cu2++Cl﹣
(3)4OH﹣﹣4e﹣=2H2O+O2↑;HPO32﹣+2H+=H3PO3
【解析】 解:(1)①2Cu2S(s)+3O2(g)═2Cu2O(s)+2SO2(g)△H=﹣768.2kJmol﹣1 , ②2Cu2O(s)+Cu2S(s)═6Cu(s)+SO2(g)△H=+116.0kJmol﹣1 , 据盖斯定律(①+②)÷3得:Cu2S(s)+O2(g)═2Cu(s)+SO2(g)△H=﹣217.4KJ/mol,所以答案是:Cu2S(s)+O2(g)═2Cu(s)+SO2(g)△H=﹣217.4KJ/mol;(2)①在c(Cl﹣)=9molL﹣1处,做一条平行与纵轴的虚线,可见溶液中主要含铜物种浓度大小关系为:c(CuCl2)>c(CuCl+)>c(CuCl3﹣)>c(Cu2+)>c(CuCl42﹣),所以答案是:c(CuCl2)>c(CuCl+)>c(CuCl3﹣);②从图上可见,在c(Cl﹣)=1molL﹣1的氯化铜溶液中,主要是Cu2+与Cl﹣结合生成CuCl+ , 加入硝酸银,氯离子浓度下降,方程式为:CuCl+═Cu2++Cl﹣ , 所以答案是:CuCl+═Cu2++Cl﹣;(3)①阳极上氢氧根离子失电子发生氧化反应,电极反应式为4OH﹣﹣4e﹣=2H2O+O2↑,所以答案是:4OH﹣﹣4e﹣=2H2O+O2↑;②产品室中HPO32﹣和氢离子结合生成亚磷酸,反应离子方程式为:HPO32﹣+2H+=H3PO3 , 所以答案是:HPO32﹣+2H+=H3PO3 .