题目内容
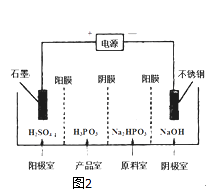
【题目】电解原理在化学工业中有广泛应用.如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题: 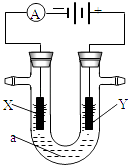
(1)若X、Y都是惰性电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞试液,则:
①电解池中X极上的电极反应式为;在X极附近观察到的现象是 .
②Y电极上的电极反应式为;检验该电极反应产物的方法是 .
(2)如用电解方法精炼粗铜,电解液a选用CuSO4溶液,则
①X电极的材料是 , 电极反应式为 .
②Y电极的材料是 , 电极反应式为 . (说明:杂质发生的电极反应不必写出)
【答案】
(1)2H++2e﹣=H2↑;放出气体,溶液变红;2Cl﹣﹣2e﹣=Cl2↑;把湿润的碘化钾淀粉试纸放在Y电极附近,试纸变蓝色
(2)纯铜;Cu2++2e﹣=Cu;粗铜;Cu﹣2e﹣=Cu2+
【解析】解:(1)①和电源的负极相连的电极X极是阴极,该电极上氢离子发生得电子的还原反应,即2H++2e﹣=H2↑,所以该电极附近氢氧根浓度增大,碱性增强,滴入几滴酚酞试液会变红,所以答案是:2H++2e﹣=H2↑;放出气体,溶液变红;②和电源的正极相连的电极Y极是阳极,该电极上氯离子发生失电子的氧化反应,即2Cl﹣﹣2e﹣=Cl2↑,氯气能使湿润的碘化钾淀粉试纸变蓝,可以用于氯气的检验,所以答案是:2Cl﹣﹣2e﹣=Cl2↑;把湿润的碘化钾淀粉试纸放在Y电极附近,试纸变蓝色;(2)①电解方法精炼粗铜,电解池的阴极材料是纯铜,电极反应为:Cu2++2e﹣=Cu,所以答案是:纯铜; Cu2++2e﹣=Cu;②电解方法精炼粗铜,电解池的阳极材料是粗铜,电极反应为:Cu﹣2e﹣=Cu2+ , 所以答案是:粗铜;Cu﹣2e﹣=Cu2+ .

练习册系列答案
相关题目