题目内容
已知在25℃,101kPa下,1g 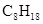 (辛烷)燃烧生成二氧化碳和液态水时放出48.40kJ热量.表示上述反应的热化学方程式正确的是( )
(辛烷)燃烧生成二氧化碳和液态水时放出48.40kJ热量.表示上述反应的热化学方程式正确的是( )
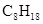 (辛烷)燃烧生成二氧化碳和液态水时放出48.40kJ热量.表示上述反应的热化学方程式正确的是( )
(辛烷)燃烧生成二氧化碳和液态水时放出48.40kJ热量.表示上述反应的热化学方程式正确的是( )A.  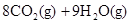 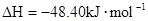 |
B.  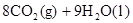 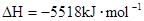 |
C.  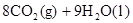 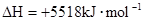 |
D.  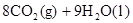 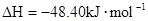 |
B
1g辛烷相当于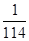 mol,1mol辛烷完全燃烧放出热量为48.40×114=5518kJ。书写热化学方程式时要注明聚集状态,注意计量数与热量数值一致,当放热时?H取负值,故B答案正确。
mol,1mol辛烷完全燃烧放出热量为48.40×114=5518kJ。书写热化学方程式时要注明聚集状态,注意计量数与热量数值一致,当放热时?H取负值,故B答案正确。
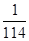 mol,1mol辛烷完全燃烧放出热量为48.40×114=5518kJ。书写热化学方程式时要注明聚集状态,注意计量数与热量数值一致,当放热时?H取负值,故B答案正确。
mol,1mol辛烷完全燃烧放出热量为48.40×114=5518kJ。书写热化学方程式时要注明聚集状态,注意计量数与热量数值一致,当放热时?H取负值,故B答案正确。
练习册系列答案
相关题目

 CH3OH(g) ΔH1
CH3OH(g) ΔH1

 2NH3(g)。当生成2molNH3时,放出热量为92kJ,在相同温度和压强下,向密闭容器中通入3mol H2和1mol N2,达到平衡时放出热量为Q,则下列关系式中正确的是
2NH3(g)。当生成2molNH3时,放出热量为92kJ,在相同温度和压强下,向密闭容器中通入3mol H2和1mol N2,达到平衡时放出热量为Q,则下列关系式中正确的是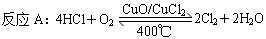
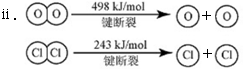
 2NH3(g) +
2NH3(g) + 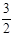 O2(g) ;△H =" a" kJ·mol—1
O2(g) ;△H =" a" kJ·mol—1 2H2O(l) ΔH = -571.6kJ·mol—1
2H2O(l) ΔH = -571.6kJ·mol—1