题目内容
[2012·北京卷,节选](6分)用Cl2生产某些含氯有机物时会产生副产物HCl。利用反应A,可实现氯的循环利用。
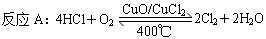
已知:i.反应A中,4 mol HCl被氧化,放出115.6 kJ的热量。
(1)H2O的电子式是____________。
(2)反应A的热化学方程式是___________________________________。
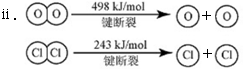
(3)断开1 mol H-O键与断开1 mol H-Cl键所需能量相差约为________kJ,H2O中H-O键比HCl中H-Cl键(填“强”或“弱”)________。
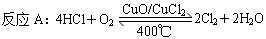
已知:i.反应A中,4 mol HCl被氧化,放出115.6 kJ的热量。

(1)H2O的电子式是____________。
(2)反应A的热化学方程式是___________________________________。
(3)断开1 mol H-O键与断开1 mol H-Cl键所需能量相差约为________kJ,H2O中H-O键比HCl中H-Cl键(填“强”或“弱”)________。
(6分)(1)
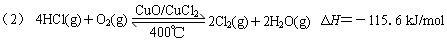
(3)32 强

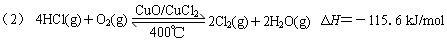
(3)32 强
(1)H2O是共价化合物,原子间通过共用电子对结合,故H2O的电子式为 。
。
(2)利用反应A与题中信息“氧化4 mol HCl放出115.6 kJ的热量可写出热化学方程式:
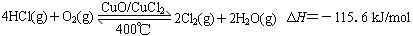 。
。
(3)设H—Cl键键能为x kJ/mol、H-O键键能为y kJ/mol,依据②中热化学方程式和题干中已知数据有:4x+498-243×2-4y=-115.6,解之得:y-x=32,说明H-O键与H-Cl键键能相差32 kJ/mol。因为“键能越大,键越牢固”,所以H-O键强于H-Cl键。
 。
。(2)利用反应A与题中信息“氧化4 mol HCl放出115.6 kJ的热量可写出热化学方程式:
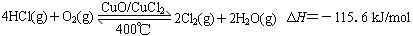 。
。(3)设H—Cl键键能为x kJ/mol、H-O键键能为y kJ/mol,依据②中热化学方程式和题干中已知数据有:4x+498-243×2-4y=-115.6,解之得:y-x=32,说明H-O键与H-Cl键键能相差32 kJ/mol。因为“键能越大,键越牢固”,所以H-O键强于H-Cl键。

练习册系列答案
 53天天练系列答案
53天天练系列答案
相关题目
 ===H2O(g) △H1=a kJ·
===H2O(g) △H1=a kJ·
 ===2H2O(g) △H2=b kJ·
===2H2O(g) △H2=b kJ· ===2H2O(l) △H4=d kJ·
===2H2O(l) △H4=d kJ·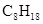 (辛烷)燃烧生成二氧化碳和液态水时放出48.40kJ热量.表示上述反应的热化学方程式正确的是( )
(辛烷)燃烧生成二氧化碳和液态水时放出48.40kJ热量.表示上述反应的热化学方程式正确的是( )

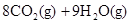
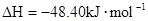
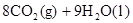
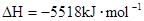
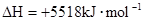

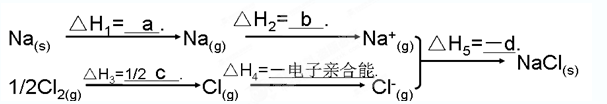
 O2 (g)
O2 (g)