题目内容
重水(D2O)是重要的核工业原料,下列说法错误的是
A.氘(D)原子核外有1个电子
B.1H与D互称同位素
C.H2O与D2O互称同素异形体
D.1H218O与D216O的相对分子质量相同
C
解析试题分析:A、氘(D)原子是指核内1个质子和1个中子的氢原子,所以核外有1个电子,正确;B、1H与D质子数相同,而中子数不同,互为同位素,正确;C、同素异形体是指同种元素对应的不同单质,H2O与D2O不是单质,错误;D、1H218O与D216O的相对分子质量都为20,正确,答案选C。
考点:考查同位素、同素异形体的概念

练习册系列答案
 津桥教育计算小状元系列答案
津桥教育计算小状元系列答案
相关题目
下列微粒半径大小比较正确的是:
| A.Na+<Mg2+<Al3+<O2- | B.S2->Cl->Na+>Al3+ |
| C.Na<Mg<Al<S | D.Ca<Rb<K<Na |
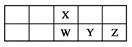
W、X、Y、Z是四种常见的短周期元素,其原子半径随原子序数变化如下图。已知W的一种核素的质量数为18,中子数为10;X和Ne原子的核外电子数相差1;Y的单质是一种常见的半导体材料;Z的非金属性在同周期元素中最强。下列说法正确的是
| A.对应简单离子半径:X>W |
| B.对应气态氢化物的稳定性Y>Z |
| C.化合物XZW既含离子键,又含共价键 |
| D.Y的氧化物能与Z的氢化物和X的最高价氧化物对应的水化物的溶液反应 |
元素在周围表中的位置,反映了元素的原子结构和元素的性质,下列说法正确的是( )
| A.同一元素不可能既表现金属性,又表现非金属性 |
| B.第三周期主族元素的最高正化合价等于它所处的主族序数 |
| C.短周期元素形成离子后,最外层都达到8电子稳定结构 |
| D.同一主族的元素的原子,最外层电子数相同,化学性质完全相同 |
已知16S、34Se位于同一主族,下列关系正确的是
| A.热稳定性:H2Se> H2S> HCl | B.原子半径:Se>P>Si |
| C.酸性:H3PO4>H2SO4>H2SeO4 | D.还原性:Se2->Br->Cl- |
下列事实中,能说明氯的非金属性比硫强的是
| A.高氯酸的酸性比亚硫酸强 | B.次氯酸的氧化性比稀硫酸强 |
| C.氯化氢比硫化氢的热稳定性好 | D.氯原子最外层电子数比硫原子多 |
短周期主族元素X、Y、Z、W的原子序数依次增大,原子半径:r(W)>r(Y)>r(Z)>r(X)。X与W同主族,Z原子最外层电子数是其内层电子总数的3倍,Z原子的核电荷数等于X、Y原子核电荷数之和。下列说法正确的是
| A.元素Z、W的简单离子的电子层结构不同 |
| B.元素Y的简单气态氢化物的热稳定性比Z的强 |
| C.仅由X、Y、Z三种元素形成的化合物的水溶液可能呈碱性 |
| D.化合物X2Z2与W2Z2所含化学键类型完全相同 |
下列各组性质的比较中正确的是
| A.酸性:HClO4<H2SO4<H3PO4 | B.碱性:Ba(OH)2>Ca(OH)2>Mg(OH)2 |
| C.稳定性:HF>HCl>PH3>H2S | D.原子半径:O>S>Na |