题目内容
【题目】I.某化学实验小组为了探究在实验室制备Cl2的过程中有水蒸气和HCl挥发出来,同时证明氯气的某些性质,某同学设计了如图所示的实验装置(氯气易溶于CCl4,HCl不溶于CCl4)。
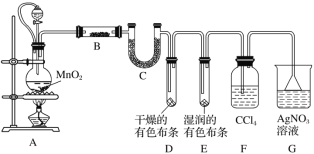
请回答下列问题:
(1)装置A中连接橡皮管的目的是_____________________________________。
(2)装置A中发生反应的离子方程式为_________________________________,装置B中盛放的试剂是___________。
(3)装置D与E中出现的不同现象说明的问题是_________________________。
(4)有同学基于实验的严谨性考虑,认为可在F、G两个装置之间再加一个装有湿润的淀粉KI试纸的装置,其目的是___________________________________。
Ⅱ.某研究性学习小组欲制备漂白粉,设计在上述装置A后连接如右图所示的组合装置:
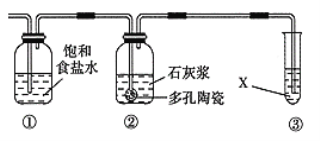
(5)装置②中发生反应的化学方程为___________________________________。
(6)制漂白粉的反应是放热反应,反应温度较高时有副反应发生,改进该实验装置以减少副反应发生的方法是___________________________________。
【答案】使内外压强相等,有利于分液漏斗中的浓盐酸顺利流下 MnO2+4H++2Cl-![]() Mn2++Cl2↑+2H2O 无水硫酸铜 氯气无漂白性,次氯酸有漂白性 验证HCl中的Cl2已经完全除去(或验证是否还含有Cl2)等同类合理答案均可 2Ca(OH)2+2Cl2=CaCl2+Ca(ClO)2+2H2O 将装置②放于冷水浴中进行实验
Mn2++Cl2↑+2H2O 无水硫酸铜 氯气无漂白性,次氯酸有漂白性 验证HCl中的Cl2已经完全除去(或验证是否还含有Cl2)等同类合理答案均可 2Ca(OH)2+2Cl2=CaCl2+Ca(ClO)2+2H2O 将装置②放于冷水浴中进行实验
【解析】
(1)联系压强与分液漏斗的作用回答;
(2)联系题意可知装置A的目的为制备Cl2,并检验有水蒸气和HCl挥发出来,联系实验室制Cl2与水蒸气的检验方法回答;
(3)D中干燥有色布条不褪色,而E中湿润有色布条褪色;
(4)装置F中CCl4的作用为吸收Cl2,防止对HCl的检验产生干扰,湿润的淀粉KI试纸可检验Cl2;
(5)装置②中试剂为石灰浆,联系漂白粉的制备方法可知装置②中应为Cl2与Ca(OH)2反应;
(6)温度较高时有副反应发生,降低温度可减少副反应发生。
(1)装置A中连接橡皮管,可使分液漏斗与圆底烧瓶压强相等,有利于有利于分液漏斗中的浓盐酸顺利流下;
(2)装置A中利用浓盐酸和MnO2混合加热制氯气,发生反应的离子方程式为:MnO2+4H++2Cl-![]() Mn2++Cl2↑+2H2O;无水硫酸铜遇到水发生反应生成蓝色硫酸铜晶体,因此装置B的目的是检验水的存在,装置内盛放的试剂是:无水硫酸铜;
Mn2++Cl2↑+2H2O;无水硫酸铜遇到水发生反应生成蓝色硫酸铜晶体,因此装置B的目的是检验水的存在,装置内盛放的试剂是:无水硫酸铜;
(3)干燥的氯气没有漂白性,D中有色布条不褪色,氯气与水反应生成的HClO具有漂白性,E中湿润的有色布条褪色;
(4)氯气易溶于有机溶剂四氯化碳,而氯化氢不溶,因此装置F的作用为吸收Cl2,G的作用为检验HCl,为避免氯气与水反应生成的盐酸,对氯化氢气体的检验带来的影响,应该在F、G两个装置之间再加一个装有湿润的淀粉KI试纸的装置,可用于检验Cl2是否被除尽;
(5)装置②中发生Cl2与Ca(OH)2制Ca(ClO)2的反应,方程式为:2Ca(OH)2+2Cl2═CaCl2+Ca(ClO)2+2H2O;
(6)制漂白粉的反应是放热反应,反应温度较高时有副反应发生,为了减少副反应发生,可将装置②放于冷水浴中降低温度来达到目的。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】煤燃烧排放的烟气含有SO2和NOx,采用NaClO2溶液作为吸收剂可同时对烟气进行脱硫、脱硝。完成下列填空:
(1)上述烟气处理过程中涉及到的化学物质组成元素中,属于第三周期元素的是___;写出N的核外电子排布式___。
(2)已知SO2分子的空间构型为折线形,则SO2为___(选填“极性”、“非极性”)分子。
(3)将含有SO2和NOx的烟气通入盛有NaClO2溶液的反应器中,反应一段时问后,测得溶液中离子浓度的有关数据如下(其他离子忽略不计):
离子 | Na+ | SO42- | NO3- | OH- | Cl- |
浓度/(mol·L-1) | 5.5×10-3 | 8.5×10-4 | y | 2.0×10-4 | 3.4×10-3 |
①反应后溶液pH___7,表中y=___mol·L-1。
②写出NaClO2溶液吸收SO2的离子方程式___。
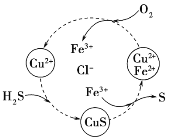
(4)烟气中的SO2还可采用氨法脱硫除去,其反应原理可用如图表示。
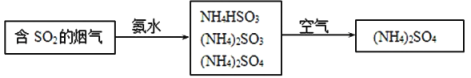
①写出SO2跟氨水反应生成NH4HSO3的化学方程式___。
②(NH4)2SO4溶液中浓度最大的离子是___。
【题目】“84消毒液”因1984年北京某医院研制使用而得名,在日常生活中使用广泛,其有效成分是NaClO。某化学研究性学习小组在实验室制备NaClO溶液,并进行性质探究和成分测定

(1)该学习小组按上图装置进行实验(部分夹持装置省去),反应一段时间后,分别取B、C瓶中的溶液进行实验,实验现象如下表。
已知:1.饱和NaClO溶液pH为11;
2.25°C时,弱酸电离常数为:H2CO3:K1=4.4×10-7,K2=4.7×10-11;HClO:K=3×10-8
B瓶 | C瓶 | |
实验1:取样,滴加紫色石蕊试液 | 变红,不褪色 | 变蓝,不褪色 |
实验2:测定溶液的pH | 3 | 12 |
回答下列问题:
①仪器a的名称_____,装置A中发生反应的离子方程式________。
②实验1中B瓶溶液中产生现象的原因是_________。
③若将C瓶溶液换成 NaHCO3溶液,按上述操作步骤进行实验,C瓶现象为:实验1中紫色石蕊试液立即褪色;实验2中溶液的pH=7。结合平衡移动原理解释紫色石蕊试液立即褪色的原因______。
(2)测定C瓶溶液中NaClO含量(单位:g/L)的实验步骤如下:
Ⅰ.取C瓶溶液20ml于锥形瓶中,加入硫酸酸化,加入过量KI溶液,盖紧瓶塞并在暗处充分反应。
Ⅱ.用0.1000mol/LNa2S2O3标准溶液滴定锥形瓶中的溶液,指示剂显示终点后,重复操作2~3次,Na2S2O3溶液的平均用量为24.00ml。(已知:I2+2S2O32-=2I-+S4O62-)
①步骤Ⅰ的C瓶中发生反应的离子方程式为_______。
②步骤Ⅱ通常选用___作指示剂,滴定至终点的现象______。
③C瓶溶液中NaClO含量为_____g/L(保留2位小数)