题目内容
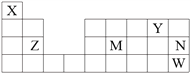
【题目】下图是工业制纯碱的部分物质转化示意图,下列说法错误的是

A. X是NH3,Y是CO2
B. M可在转化流程中循环利用
C. 若是联合制碱法,则L的主要成分是NH4Cl
D. 若是氨碱法,溶液c可在转化流程中循环利用
【答案】D
【解析】
A.联合制碱法与氨碱法其原理都是NH3+CO2+H2O+NaCl(饱和)=NaHCO3↓+NH4Cl,2NaHCO3![]() Na2CO3+H2O+CO2↑,NH3极易溶于水且溶液呈弱碱性,再通入CO2使之更多地转化为HCO3-,故工业上可先向饱和食盐水中通入NH3后再通入CO2制NaHCO3,所以X是NH3,Y是CO2,故A正确;B.图中的沉淀为碳酸氢钠,碳酸氢钠受热分解2NaHCO3
Na2CO3+H2O+CO2↑,NH3极易溶于水且溶液呈弱碱性,再通入CO2使之更多地转化为HCO3-,故工业上可先向饱和食盐水中通入NH3后再通入CO2制NaHCO3,所以X是NH3,Y是CO2,故A正确;B.图中的沉淀为碳酸氢钠,碳酸氢钠受热分解2NaHCO3![]() Na2CO3+H2O+CO2↑,M为二氧化碳,二氧化碳是反应的原料同时也是反应的副产物,可以循环利用,故B正确;C.若是联碱法,其滤液是含有氯化铵和氯化钠的溶液,第二个过程是从含有氯化铵和氯化钠的滤液中结晶沉淀出氯化铵晶体,由于氯化铵在常温下的溶解度比氯化钠要大,低温时的溶解度则比氯化钠小,而且氯化铵在氯化钠的浓溶液里的溶解度要比在水里的溶解度小得多,所以在低温条件下,向滤液中加入细粉状的氯化钠,并通入氨气,可以使氯化铵单独结晶沉淀析出,经过滤、洗涤和干燥即得氯化铵产品,所以L的主要成分是氯化铵,故C正确;D.先使氨气X通入饱和食盐水中而成氨盐水,再通入二氧化碳Y生成溶解度较小的碳酸氢钠沉淀和氯化铵溶液,含有氯化铵的滤液b与石灰乳混合加热,CaO+H2O=Ca(OH)2,2NH4Cl+Ca(OH)2
Na2CO3+H2O+CO2↑,M为二氧化碳,二氧化碳是反应的原料同时也是反应的副产物,可以循环利用,故B正确;C.若是联碱法,其滤液是含有氯化铵和氯化钠的溶液,第二个过程是从含有氯化铵和氯化钠的滤液中结晶沉淀出氯化铵晶体,由于氯化铵在常温下的溶解度比氯化钠要大,低温时的溶解度则比氯化钠小,而且氯化铵在氯化钠的浓溶液里的溶解度要比在水里的溶解度小得多,所以在低温条件下,向滤液中加入细粉状的氯化钠,并通入氨气,可以使氯化铵单独结晶沉淀析出,经过滤、洗涤和干燥即得氯化铵产品,所以L的主要成分是氯化铵,故C正确;D.先使氨气X通入饱和食盐水中而成氨盐水,再通入二氧化碳Y生成溶解度较小的碳酸氢钠沉淀和氯化铵溶液,含有氯化铵的滤液b与石灰乳混合加热,CaO+H2O=Ca(OH)2,2NH4Cl+Ca(OH)2![]() CaCl2+2NH3↑+2H2O,所放出的氨气L可回收循环使用,故D错误;故答案为D。
CaCl2+2NH3↑+2H2O,所放出的氨气L可回收循环使用,故D错误;故答案为D。

 小题狂做系列答案
小题狂做系列答案【题目】中国科学家用金属钠和CO2在一定条件下制得了金刚石:4 Na + 3CO2![]() 2 Na2CO3 + C(金刚石),以下是一些物质的熔沸点数据(常压):
2 Na2CO3 + C(金刚石),以下是一些物质的熔沸点数据(常压):
钠 | Na2CO3 | 金刚石 | 石墨 | |
熔点(℃) | 97.8 | 851 | 3550 | 3850 |
沸点(℃) | 882.9 | 1850(分解产生CO2) | ---- | 4250 |
(1)若反应在常压、890℃下进行,写出该反应的平衡常数表达式_____________________,若3v正(Na)=4v逆(CO2),则_____(选填序号)。
a.反应肯定达到平衡 b.反应可能达到平衡 c.反应肯定未达平衡
(2)若反应在10L密闭容器、常压下进行,5min内,测得金刚石的质量增加了6 g,该时间段内v(CO2)=______________,若反应温度由890℃升高到1860℃,则容器内气体的平均相对分子质量将________(选填“增大”、“减小”或“不变”) 。
(3)反应中还有石墨生成,已知:C(石墨)![]() C(金刚石),若升高温度,生成的碳单质中,金刚石的含量将增大,则该反应的正反应是_________反应(填“吸热”或“放热”)。
C(金刚石),若升高温度,生成的碳单质中,金刚石的含量将增大,则该反应的正反应是_________反应(填“吸热”或“放热”)。
(4)碳酸钠溶液中滴入盐酸的反应过程如右图所示,反应至A点时,未产生二氧化碳,请用离子方程式解释原因:_________________,继续滴加盐酸,反应至B点,B点溶液中溶质的化学式是__________。