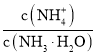题目内容
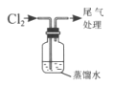
【题目】化学小组同学为探究氯水的成分及性质进行了如下实验:
实验① | 实验② | 实验③ | 实验④ | 实验⑤ | |
实验操作(氯水均为新制) |
|
|
|
|
|
实验现象 | 蒸馏水由无色逐渐变为浅黄绿色 | 溶液变蓝 | 石蕊溶液先变红,后褪色 | 产生白色沉淀 | 产生大量无色气泡 |
(试管中溶液均为1mL,均滴入氯水5滴)
(1)证明氯水中含有Cl-的是实验__(填序号),用离子方程式表示该实验中涉及的反应__。
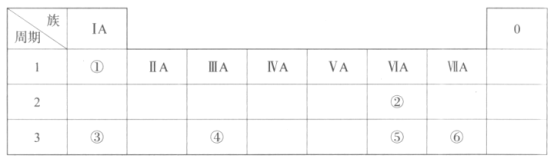
(2)由实验②的现象可推断非金属性:Cl__I(填“>”或“<”),由原子结构解释其原因:Cl和I同主族,__,得电子能力:Cl>I(请补充完整)。
(3)实验③中溶液变红是由于溶液中含有__(填微粒符号,下同);使溶液褪色的微粒是__。
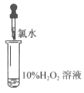
(4)同学们根据“H2O2在催化剂作用下可发生分解”的性质,认为实验⑤中现象不一定说明氧化性Cl2>H2O2。为证实Cl2将H2O2氧化,可继续补充实验:__(填操作、现象)。
(5)同学们发现久置的氯水会失去漂白性,溶液由黄绿色变为无色。为探究氯水失效的原因,进行实验:用强光照射盛有氯水的密闭广口瓶,并用传感器测定广口瓶中数据,得到如图曲线。

解释上两图中曲线变化的原因__。若在上述整个实验过程中测定溶液的pH,pH的变化是__。
【答案】④ Cl2+H2O=H++Cl-+HClO、Cl-+Ag+=AgCl↓ > 核外电子层数:Cl<I,原子半径:Cl<I H+(或HCl) HClO 反应后向溶液中加入1mL2%AgNO3溶液,产生的沉淀量明显大于实验④ 由于2HClO![]() 2HCl+O2↑,使O2体积分数增加;Cl2与水不断反应和HClO分解生成的HCl使溶液中c(Cl-)增大 溶液的pH随时间增长逐渐减小(最终不变)
2HCl+O2↑,使O2体积分数增加;Cl2与水不断反应和HClO分解生成的HCl使溶液中c(Cl-)增大 溶液的pH随时间增长逐渐减小(最终不变)
【解析】
实验①能说明氯气易溶于水;实验②证明氯气能从KI中置换出I2;实验③说明氯水具有酸性且有漂白性;实验④说明氯水中含有Cl-,与硝酸银反应生成氯化银的白色沉淀;实验⑤中氯气与过氧化氢反应生成无色气体氧气,其化学反应方程式为:H2O2+Cl2=2HCl+O2。
(1)氯气溶于水,且一部分氯气与水反应,其离子反应方程式为:Cl2+H2O![]() H++Cl-+HClO,实验④证明氯水中含有Cl-,与硝酸银反应生成氯化银的白色沉淀,其离子反应方程式为:Cl-+Ag+=AgCl↓,故答案为:④;Cl2+H2O=H++Cl-+HClO、Cl-+Ag+=AgCl↓;
H++Cl-+HClO,实验④证明氯水中含有Cl-,与硝酸银反应生成氯化银的白色沉淀,其离子反应方程式为:Cl-+Ag+=AgCl↓,故答案为:④;Cl2+H2O=H++Cl-+HClO、Cl-+Ag+=AgCl↓;
(2)实验②中淀粉变蓝,说明氯气与KI发生反应置换出I2,其反应方程式为:Cl2+2KI=2KCl+I2,可推断非金属性:Cl>I。由原子结构解释其原因:Cl和I同主族,核外电子层数:Cl<I,原子半径:Cl<I,得电子能力:Cl>I,故答案为:>;核外电子层数:Cl<I,原子半径:Cl<I;
(3)氯气溶于水,且一部分氯气与水反应,其离子反应方程式为:Cl2+H2O![]() H++Cl-+HClO,氯水中含有H+,溶液显酸性,石蕊溶液先变红,又因为HClO具有强氧化性,使红色石蕊褪色,故答案为:H+(或HCl); HClO;
H++Cl-+HClO,氯水中含有H+,溶液显酸性,石蕊溶液先变红,又因为HClO具有强氧化性,使红色石蕊褪色,故答案为:H+(或HCl); HClO;
(4)实验⑤中氯气氧化过氧化氢反应生成无色气体氧气,其化学反应方程式为:H2O2+Cl2=2HCl+O2,反应后向溶液中加入1mL2%AgNO3溶液,产生的沉淀量明显大于实验④,证实Cl2将H2O2氧化,故答案为:反应后向溶液中加入1mL2%AgNO3溶液,产生的沉淀量明显大于实验④;
(5)氯气溶于水,且一部分氯气与水反应,其离子反应方程式为:Cl2+H2O![]() H++Cl-+HClO,由于2HClO
H++Cl-+HClO,由于2HClO![]() 2HCl+O2↑,使O2体积分数增加,Cl2与水不断反应和HClO分解生成的HCl溶液的pH随时间增长逐渐减小(最终不变),c(Cl-)增大,故答案为:由于
2HCl+O2↑,使O2体积分数增加,Cl2与水不断反应和HClO分解生成的HCl溶液的pH随时间增长逐渐减小(最终不变),c(Cl-)增大,故答案为:由于
2HClO![]() 2HCl+O2↑,使O2体积分数增加;Cl2与水不断反应和HClO分解生成的HCl使溶液中c(Cl-)增大;溶液的pH随时间增长逐渐减小(最终不变)。
2HCl+O2↑,使O2体积分数增加;Cl2与水不断反应和HClO分解生成的HCl使溶液中c(Cl-)增大;溶液的pH随时间增长逐渐减小(最终不变)。

【题目】50 mL 1.0molL﹣1盐酸跟50 mL 1.1 molL﹣1氢氧化钠溶液在图所示装置中进行中和反应,并通过测定反应过程中所放出的热量来计算中和热。试回答下列问题:
(1)实验时不能用铜丝搅拌棒代替环形玻璃搅拌棒的理由是___________。

(2)大烧杯上如不盖硬纸板,对求得中和热数值的影响是_____(填“偏高”“偏低”或“无影响”)。
(3)如果改用60 mL 1.0 molL﹣1盐酸跟50 mL 1.1 molL﹣1氢氧化钠溶液进行反应,则与上述实验相比,所放热量_____(填“增加”“减少”或“不变”);所求中和热数值_____(填“增加”“减少”或“不变”)。
(4)_____(填“能”或“不能”)用Ba(OH)2和硫酸代替盐酸和氢氧化钠溶液。
(5)Q=cm△t,其中Q表示此中和反应放出的热量,m表示反应后混合液的质量,c表示反应后混合溶液的比热容,△t表示反应前后溶液的温度的差值。该实验小组做了三次实验,每次取溶液各50 mL,并记录如下原始数据:
实验序号 | 起始温度t1/℃ | 终止温度t2/℃ | 温差(t2﹣t1)/℃ |
1 | 25.0 | 32.6 | |
2 | 25.1 | 31.8 | |
3 | 25.1 | 31.9 |
已知盐酸、NaOH溶液密度近似为1.00 gcm﹣3,中和后混合液的比热容c=4.184×10﹣3kJg﹣1℃﹣1则该反应的中和热为△H=_____(保留小数点后一位)。
(6)上述实验数值结果与57.3 kJmol﹣1有偏差,产生偏差的原因可能是_____(填字母)。
a.实验装置保温、隔热效果差 b.量取盐酸的体积时仰视读数
c.分多次把NaOH溶液倒入盛有盐酸的小烧杯中
d.用温度计测定NaOH溶液起始温度后直接测定HCl溶液的温度