题目内容
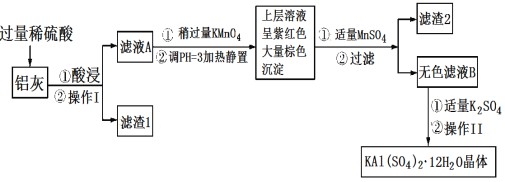
【题目】现有NaCl、Na2SO4和NaNO3的混合物,选择适当的试剂除去杂质,从而得到纯净的NaNO3晶体,相应的实验流程如图所示。

请回答下列问题:
(1)写出实验流程中下列物质的化学式:试剂X__,沉淀A___。
(2)上述实验流程中①②③步均要进行的实验操作是__(填操作名称)。
(3)上述实验流程中加入过量Na2CO3溶液的目的是__________。
(4)按此实验方案得到的溶液3中肯定含有____(填化学式)杂质。为了解决这个问题,可以向溶液3中加入适量的__(填化学式)。
(5)在①步操作中如何证明加的BaCl2溶液已过量?________。
【答案】AgNO3 BaSO4 过滤 除去过量的Ba2+和Ag+ Na2CO3 HNO3 取混合溶液的上层清液少量于试管中,用胶头滴管继续滴加少量BaCl2溶液,如无明显现象,则证明所加的BaCl2已过量
【解析】
由流程图可知,①中加过量氯化钡,硫酸根离子转化为硫酸钡沉淀,则沉淀A为BaSO4,溶液1中含氯化钠、硝酸钠和过量的氯化钡,③应该是沉淀钡离子,则②为沉淀氯离子,因此②中加AgNO3后氯离子转化氯化银沉淀,沉淀B为AgCl,溶液2中含硝酸钠、硝酸银、硝酸钡,③中加入过量的碳酸钠,钡离子,银离子转化为沉淀,沉淀C为碳酸钡、碳酸银,溶液3为硝酸钠和碳酸钠,据此分析解答。
(1)由上述分析可知,试剂X为AgNO3,沉淀A为BaSO4,故答案为:AgNO3;BaSO4;
(2)流程中①②③步均生成沉淀,都需要进行过滤操作,故答案为:过滤;
(3)加入过量的Na2CO3的目的是使溶液中过量的Ag+、Ba2+完全沉淀,故答案为:除去过量的Ba2+和Ag+;
(4)溶液3为硝酸钠和碳酸钠,按此实验方案得到的溶液3中肯定含有Na2CO3杂质,可加适量的稀硝酸后蒸发结晶或加热冷却结晶得到纯净的硝酸钠,故答案为:Na2CO3;稀HNO3;
(5)在①步操作中证明加的BaCl2溶液已过量,只需要检验溶液中不存在硫酸根离子即可,方法为:取混合溶液的上层清液少量于试管中,用胶头滴管继续滴加少量BaCl2溶液,如无明显现象,则证明所加的BaCl2已过量,故答案为:取混合溶液的上层清液少量于试管中,用胶头滴管继续滴加少量BaCl2溶液,如无明显现象,则证明所加的BaCl2已过量。

 阅读快车系列答案
阅读快车系列答案