题目内容
下列不能达到实验目的的是
| 序号 | 实验内容 | 实验目的 |
| A | 用石墨电极电解Mg(NO3)2、Cu( NO3)2的混合液 | 比较确定铜和镁的金属活动性强弱 |
| B | 测同温同浓度Na2CO3和Na2SiO3水溶液的pH | 确定碳和硅两元素非金属性强弱 |
| C | 室温下,用pH试纸测定浓度为0.1mol·L-1NaClO溶液和0.1mol·L-1CH3COONa溶液的pH | 比较HClO和CH3COOH的酸性强弱 |
| D | 室温下,分别向2支试管中加入相同体积、相同浓度的Na2S2O3溶液,再分别加入相同体积不同浓度的稀硫酸 | 研究浓度对反应速率的影响 |
C
试题分析:A、根据金属阳离子在阴极放电的先后顺序可以判断金属活动性强弱,铜离子先放电,金属铜活动性就弱,正确;B、根据“越弱越水解”盐类水解规律,最高价含氧酸的酸性越弱其对应的酸根离子水解程度越大,pH越大,进一步推出其非金属性越弱,正确;C、用pH试纸测定浓度为0.1mol·L-1NaClO,最终试纸漂白,实验达不到目的,错误;D、控制单一变量法,改变浓度,能够达到实验目的,正确。

练习册系列答案
相关题目

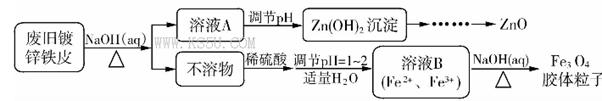
 Fe3O4(胶体)+S4O62-+H2O
Fe3O4(胶体)+S4O62-+H2O