题目内容
(2010?沈阳二模)下列实验过程中产生的现象与对应的图形正确的是( )
分析:A.根据反应AlO2-+H++H2O═Al(OH)3↓,Al(OH)3↓+3H+═Al3++3H2O判断;
B.根据反应Br2+SO2+2H2O═H2SO4+2HBr判断;
C.醋酸为弱电解质,盐酸为强电解质,二者加水稀释时的pH变化不同,无论怎么稀释,溶液都呈酸性;
D.氨气与醋酸反应生成强电解质醋酸铵.
B.根据反应Br2+SO2+2H2O═H2SO4+2HBr判断;
C.醋酸为弱电解质,盐酸为强电解质,二者加水稀释时的pH变化不同,无论怎么稀释,溶液都呈酸性;
D.氨气与醋酸反应生成强电解质醋酸铵.
解答:解:A.在NaAlO2溶液中加入盐酸,发生反应分别为AlO2-+H++H2O═Al(OH)3↓,Al(OH)3↓+3H+═Al3++3H2O,反应开始时有沉淀生成,然后沉淀溶解,故A正确;
B.SO2气体通入溴水中,发生反应Br2+SO2+2H2O═H2SO4+2HBr,反应后溶液酸性增强,pH减小,但溴水溶液呈酸性,开始时pH<7,故B错误;
C.醋酸为弱酸,加水稀释时进一步电离,pH变化较盐酸小,但无论怎么稀释,溶液都成酸性,不可能呈碱性,故C错误;
D.氨气通入醋酸溶液中,反应生成强电解质醋酸铵,溶液导电能力增强,故D错误.
故选A.
B.SO2气体通入溴水中,发生反应Br2+SO2+2H2O═H2SO4+2HBr,反应后溶液酸性增强,pH减小,但溴水溶液呈酸性,开始时pH<7,故B错误;
C.醋酸为弱酸,加水稀释时进一步电离,pH变化较盐酸小,但无论怎么稀释,溶液都成酸性,不可能呈碱性,故C错误;
D.氨气通入醋酸溶液中,反应生成强电解质醋酸铵,溶液导电能力增强,故D错误.
故选A.
点评:本题考查较为综合,涉及物质的性质和弱电解质的电离,题目难度中等,易错点为BD,注意看准图象曲线的变化.

练习册系列答案
相关题目
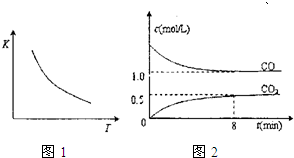 (2010?沈阳二模)一定条件下某密闭容器中发生反应:FeO(s)+CO(g)?Fe(s)+CO2(g),已知该反应的平衡常数(K)的与温度(T)的关系如图1,图2是T1温度下该反应的c-t关系图象.则下列说法正确的是( )
(2010?沈阳二模)一定条件下某密闭容器中发生反应:FeO(s)+CO(g)?Fe(s)+CO2(g),已知该反应的平衡常数(K)的与温度(T)的关系如图1,图2是T1温度下该反应的c-t关系图象.则下列说法正确的是( )