题目内容
4.下列分离与提纯物质的实验操作中错误的是( )| A. | 萃取时,要求萃取剂的密度比水的密度大 | |
| B. | 蒸馏时,温度计水银球与蒸馏烧瓶支管口相平 | |
| C. | 过滤时,要将待过滤混合物转移到漏斗中 | |
| D. | 分液时,分液漏斗的下口必须紧贴在烧杯壁上 |
分析 A.萃取剂的选择与密度无关;
B.温度计水银球应靠近蒸馏烧瓶的支管口处;
C.要将待过滤混合物用玻璃棒引流转移到漏斗中;
D.漏斗下端管口要和盛滤液的烧杯内壁相靠,使滤液能沿着烧杯内壁流下.
解答 解:A.萃取的基本原则两种溶剂互不相溶,且溶质在一种溶剂中的溶解度比在另一种大的多.密度也可以比水小,故A错误;
B.蒸馏操作时,温度计水银球应靠近蒸馏烧瓶的支管口处,故B正确;
C.过滤时,要将待过滤混合物用玻璃棒引流转移到漏斗中,故C正确;
D.漏斗下端管口要和盛滤液的烧杯内壁相靠,使滤液能沿着烧杯内壁流下,防止液体溅出,故D正确.
故选A.
点评 本题考查物质的分离、提纯,侧重于学生的分析能力和实验能力的考查,为高频考点,注意把握实验操作的方法,难度不大.

练习册系列答案
相关题目
14.雷美替胺是首个没有列为特殊管制的非成瘾失眠症治疗药物,合成该有机物过程中涉及如下转化,下列说法正确的是( )


| A. | 可用溴水区分化合物Ⅱ和化合物Ⅲ | |
| B. | 化合物Ⅰ中所有原子可能在同一平面 | |
| C. | 化合物Ⅰ、Ⅱ、Ⅲ均能与NaHCO3溶液发生反应 | |
| D. | 1 mol化合物Ⅰ最多能与3 mol H2发生加成反应 |
15. 氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用.
氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用.
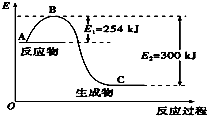
(1)如图是N2(g)和H2(g)反应生成1mol NH3(g)过程中能量变化示意图,A代表的含义代表反应物的总能量A与C差值代表的含义代表反应热的大小.请写出N2和H2反应的热化学方程式:N2(g)+3H2(g)?2NH3(g)△H=-92KJ/mol.反应过程中加入正向催化剂,E1和E2变化情况变小(变大,变小,不变),△H变化情况不变(变大,变小,不变)假设此反应在密闭容器中反应过程中活化分子百分数变化情况变大(变大,变小,不变).
(2)若已知下列数据
试根据表中及图中数据计算N-H的键能为390kJ•mol-1.
(3)用NH3催化还原NOx还可以消除氮氧化物的污染.
例如:4NH3(g)+3O2(g)═2N2(g)+6H2O(g)△H1=-a kJ•mol-1 ①
N2(g)+O2(g)═2NO(g)△H2=-b kJ•mol-1 ②
若1mol NH3还原NO至N2,并生成水蒸气,则该反应过程中的反应热△H3=$\frac{(3b-a)}{4}$kJ•mol-1(用含a、b的式子表示).
 氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用.
氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用.(1)如图是N2(g)和H2(g)反应生成1mol NH3(g)过程中能量变化示意图,A代表的含义代表反应物的总能量A与C差值代表的含义代表反应热的大小.请写出N2和H2反应的热化学方程式:N2(g)+3H2(g)?2NH3(g)△H=-92KJ/mol.反应过程中加入正向催化剂,E1和E2变化情况变小(变大,变小,不变),△H变化情况不变(变大,变小,不变)假设此反应在密闭容器中反应过程中活化分子百分数变化情况变大(变大,变小,不变).
(2)若已知下列数据
| 化学键 | H-H | N≡N |
| 键能/kJ•mol-1 | 435 | 943 |
(3)用NH3催化还原NOx还可以消除氮氧化物的污染.
例如:4NH3(g)+3O2(g)═2N2(g)+6H2O(g)△H1=-a kJ•mol-1 ①
N2(g)+O2(g)═2NO(g)△H2=-b kJ•mol-1 ②
若1mol NH3还原NO至N2,并生成水蒸气,则该反应过程中的反应热△H3=$\frac{(3b-a)}{4}$kJ•mol-1(用含a、b的式子表示).
12.元素性质随原子序数的递增呈周期性变化的本质是( )
| A. | 原子核外电子排布呈现周期性变化 | |
| B. | 原子的电子层数增多 | |
| C. | 元素的相对原子质量逐渐增大,量变引起质变 | |
| D. | 原子半径呈周期性变化 |
19.难溶电解质AB2的饱和溶液中[A2+]=x mol•L-1,[B-]=y mol•L-1,则Ksp值为( )
| A. | 0.5xy2 | B. | xy | C. | xy2 | D. | 4xy2 |
9.人们在研究金星大气成分时发现金星大气中有一种称为羰基硫(COS)的分子,其结构与CO2类似,羰基硫是一种与生命密切相关的物质,下列有关COS的推测不正确的是( )
| A. | COS分子是含有极性键的极性分子 | |
| B. | COS的电子式为: | |
| C. | COS的分子中所有原子满足8电子稳定结构 | |
| D. | COS分子中三个原子处于同一直线上 |
16.中学化学中很多“规律”都有其适用范围,下列根据有关“规律”推出的结论合理的是( )
| A. | 根据同周期元素的第一电离能变化趋势,推出Al的第一电离能比Mg大 | |
| B. | 根据主族元素最高正化合价与族序数的关系,推出卤族元素最高正价都是+7 | |
| C. | 根据同周期元素的电负性变化趋势,推出Ar的电负性比Cl大 | |
| D. | 根据较强酸可以制取较弱酸的规律,推出CO2通入NaClO溶液中能生成HClO |
13.下列说法中不正确的是( )
| A. | 浓硫酸能与灼热的木炭反应,生成二氧化碳和二氧化硫 | |
| B. | 浓硫酸具有吸水性,在实验室中常用作干燥剂 | |
| C. | 常温下,可以用铁质或铝质容器储存浓硫酸或浓硝酸 | |
| D. | 浓硫酸与铜反应产生的气体对环境无影响 |
14.当光束通过某红褐色液体时,从侧面可观察到一条光亮的“通路”,该红褐色液体是( )
| A. | 溶液 | B. | 胶体 | C. | 悬浊液 | D. | 乳浊液 |