题目内容
【题目】设NA为阿伏加德罗常数的值。下列有关叙述正确的是![]()
A. 6.8 g熔融的KHS04中含有的离子数为0.15 NA
B. 标准状况下,11.2 L乙酸中含有的碳碳键数为0.5NA
C. N2(g)+3H2(g)=2NH3(g)△H=-92.4 kJ/mol,当转移的电子数为6NA时,该反应放 出 92.4 kJ的热量
D. 常温常压下,4.4gCO2和N2O混合气体中含有的原子总数为0.6NA
【答案】C
【解析】熔融的KHS04中含有钾离子和硫酸氢根离子,6.8 g熔融的KHS04(即0.05mol)中含有的离子数为0.05×2×NA=0.1 NA, A错误;乙酸在标况下为固态,无法用气体摩尔体积进行计算,B错误;根据N2(g)+3H2(g)=2NH3(g)△H=-92.4 kJ/mol可知,当反应转移6NA电子时,反应放出的热量为92.4 kJ,C正确;4.4gCO2气体的量为0.1 mol,含有原子总数为0.3 NA; 4.4gN2O气体的量为0.1 mol,含有原子总数为0.3 NA;所以4.4gCO2和N2O混合气体中含有的原子总数为0.3NA,D错误;正确选项C。

【题目】碳酸钙、盐酸是中学化学实验中的常用试剂.
(1)甲同学拟测定CaCO3固体与过量0.1molL﹣1 HCl的反应速率.
①该反应的离子方程式为 .
②设计实验方案:通过测量计算反应速率
(2)乙同学拟用如图装置探究固体表面积和反应物浓度对化学反应速率的影响.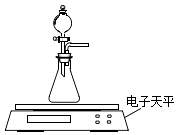
电子天平限选试剂与用品:0.1molL﹣1 HCl、颗粒状CaCO3、粉末状CaCO3、蒸馏水、量筒、秒表
(i)设计实验方案:在反应物浓度或固体表面积不同的条件下,测定
(要求所测得的数据能直接体现反应速率大小).
(ⅱ) 根据(i)中设计的实验测定方案,拟定实验表格,完整体现实验方案.列出所用试剂的用量、待测物理量;数据用字母a、b、c、d表示.
已知实验1和2探究固体表面积对反应速率的影响;
实验1和3探究反应物浓度对反应速率的影响.
写出表中①﹣⑥所代表的必要数据或物理量
物理量 | V(0.1molL﹣1 HCl)/mL | m(颗粒状CaCO3)/g | m(粉末状CaCO3)/g | V(蒸馏水)/mL | ⑤ | ⑥ |
实验1 | a | b | 0 | c | d | |
实验2 | ① | 0 | ③ | c | d | |
实验3 | c | ② | 0 | ④ | d |
【题目】在一定温度下,体积为2L的密闭容器中,NO2和N2O4之间发生反应:2NO2(g)(红棕色)![]() N2O4g)(无色),如图所示.
N2O4g)(无色),如图所示.

(1)曲线 (填“X”或“Y”)表示NO2的物质的量随时间的变化曲线.
(2)若降低温度,则v(正) ,v(逆) .(填“加快”或“减慢”或“不变”).
(3)若上述反应在甲、乙两个相同容器内同时进行,分别测得甲中v(NO2)=0.3mol/(Ls),乙中v(N2O4)=6mol/(Lmin),则 中反应更快.
(4)在0到3min中内N2O4的反应速率为 .
(5)下列叙述能说明该反应已达到化学平衡状态的是(填标号) ;
A.v(NO2)=2v(N2O4) |
B.容器内压强不再发生变化 |
C.X的体积分数不再发生变化 |
D.容器内气体原子总数不再发生变化 |
E.相同时间内消耗n mol的Y的同时生成2n mol的X
F.相同时间内消耗n mol的Y的同时消耗2n mol的X.