题目内容
根据元素周期表1~20号元素的性质和递变规律,回答下列问题。
(1)属于金属元素的有 种,金属性最强的元素与氧气反应生成的化合物有 (填两种化合物的化学式)。
(2)属于稀有气体的是 (填元素符号,下同)。
(3)形成化合物种类最多的两种元素是 。
(4)第三周期中,原子半径最大的是(稀有气体除外) 。
(5)推测Si、N最简单氢化物的稳定性 大于 (填化学式)。
(1)7 K2O、K2O2(KO2也可以)
(2)He、Ne、Ar
(3)C、H
(4)Na
(5)NH3 SiH4
解析

练习册系列答案
相关题目
下表为元素周期表的一部分,请回答有关问题:
| | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | | | | | ① | ② | ③ | |
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ | |
(1)表中最活泼的金属是 ,非金属性最强的元素是 (填写元素符号)。
(2)表中能形成两性氢氧化物的元素名称是 ,写出该元素的氢氧化物与④的最高价氧化物对应水化物反应的离子方程式: 。
(3)元素⑨和元素⑩的最高价氧化物的水化物中酸性较强是 (用化学式表示)。
(4)元素⑩与元素⑤形成的化合物属于 (填 “共价”或“离子”)化合物。
(5)请画出元素②的原子结构示意图为 ,元素①的单质在常温下化学性质稳定,通常可以做保护气,请用电子式表示其分子 。
A、B、C、D、E、F六种短周期主族元素,原子序数依次增大。
| 元素 | 信息 |
| B | 其单质在常温下为双原子分子,与A可形成分 子X,X的水溶液呈碱性 |
| D | 其简单阳离子与X具有相同电子数,且是同周 期中简单阳离子中半径最小的 |
| E | 元素原子最外层比次外层少2个电子 |
| C、F | 两种元素的原子最外层共有13个电子 |
则:(1)B的原子结构示意图为 。
(2)B、C、E分别与A形成的化合物中最稳定的是 (写化学式)。
(3)C与D形成的化合物的化学式是 ,它的性质决定了它在物质的分类中应属于 ;请写出该化合物对应水化物电离的方程式 。
(4)F的单质在反应中常作 剂,该单质的水溶液与E的低价氧化物反应的离子方程式 。
(1)可正确表示原子轨道的是 。
| A.2s | B.2d | C.2px | D.3f |
(3)下列物质变化,只与范德华力有关的是 。
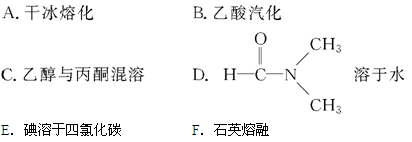
(4)下列物质中,只含有极性键的分子是 ,既含离子键又含共价键的化合物是 ;只存在σ键的分子是 ,同时存在σ键和π键的分子是 。
AN2;BCO2;CCH2Cl2;DC2H4;EC2H6;FCaCl2;GNH4Cl
(5)用“>”、“<”或“=”填空:
第一电离能的大小:Mg Al;熔点的高低:KCl MgO。
元素周期表是学习化学的重要工具,它隐含着许多信息和规律。下表所列是五种短周期元素的原子半径及主要化合价(已知铍的原子半径为0.089 nm)。
| 元素代号 | A | B | C | D | E |
| 原子半径/nm | 0.16 | 0.143 | 0.102 | 0.099 | 0.074 |
| 主要化合价 | +2 | +3 | +6,-2 | -1 | -2 |
(1)用元素代号标出它们在周期表中的对应位置(以下为周期表的一部分)。
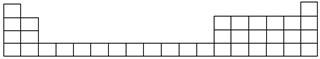
(2)B元素处于周期表中________周期________族。
(3)B的最高价氧化物的水化物与C的最高价氧化物的水化物反应的离子方程式为______________________________________________。
(4)上述五种元素的最高价氧化物对应水化物中酸性最强的是________(填化学式)。
(5)C、E形成的化合物为________(填化学式)。
 , 试回答:
, 试回答: 化合物一
化合物一 最高价氧化物
最高价氧化物