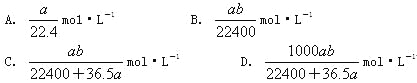��Ŀ����
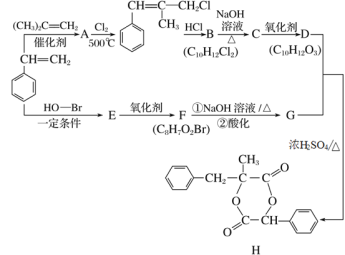
����Ŀ��A��I�ֱ��ʾ��ѧ��ѧ�г�����һ�����ʣ�����֮�����ϵ����ͼ��ʾ(���ַ�Ӧ�������û���г�)����֪HΪ��̬�����A��I���ǽ������ʣ�F�Ǻ��ɫ������ˮ�ij�������A��B��C��D��E��F���������о���ͬһ��Ԫ�ء�
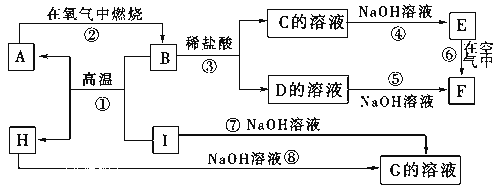
����д���пհף�
��1��A��B��C��D��E��F����������������ͬһ��Ԫ�ص�������________��
��2����Ӧ�۵����ӷ���ʽΪ________________________
��Ӧ��Ļ�ѧ����ʽΪ_____________________________________
��3����Ӧ�����е�������______________________________��
���𰸡� �� Fe3O4+8H+=2Fe3++Fe2+ +4H2O Al2O3��2NaOH��2NaAlO2��H2O �Ȳ�����ɫ������������Ϊ����ɫ�����ձ�Ϊ���ɫ
��������HΪ����Ԫ�صĹ�̬��������H�ܺ�����������Һ��Ӧ����G����H��Al2O3��I�ܺ�����������Һ��Ӧ����G����I��Al��G��NaAlO2��Al��B���ڸ����·�Ӧ����A��A����������ȼ������B�����ڸ������ܷ������ȷ�Ӧ����B�ǽ�����������A�ǽ���������B�����ᷴӦ����C��D��C���������Ʒ�Ӧ����E��D�Ͱ�ˮ��Ӧ����F��E�ڿ����з�Ӧ����F��˵��E���ȶ����ױ�������������A��B��C��D��E��F���������о���ͬһ��Ԫ��,��A��Fe��BΪFe3O4,CΪFeCl2,DΪFeCl3,EΪFe(OH)2,FΪ, Fe(OH)3��
(1)A��B��C��D��E��F����������������ͬһ��Ԫ�ص�������������ȷ����:����
(2)��Ӧ��Ϊ������������ϡ���ᷴӦ�����Ȼ��������Ȼ��������ӷ���ʽΪ��Fe3O4+8H+=2Fe3++Fe2+ +4H2O ����Ϊ������������������Һ��Ӧ����ƫ�����ƺ�ˮ����ѧ����ʽΪ��Al2O3��2NaOH��2NaAlO2��H2O����ȷ����Fe3O4+8H+=2Fe3++Fe2+ +4H2O��Al2O3��2NaOH��2NaAlO2��H2O��
��3����Ӧ(6)���������������ȶ��ױ�������������������������Ӧ���������ɰ�ɫ����Ѹ�ٱ仯Ϊ����ɫ���仯Ϊ���ɫ����ȷ�����Ȳ�����ɫ������������Ϊ����ɫ�����ձ�Ϊ���ɫ��

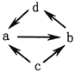
����Ŀ�����и�������֮��ͨ��һ������ʵ����ͼ��ʾת������( )
���ʱ�� | ����ת����ϵ | a | b | c | d |
�� |
| Na2O | Na2O2 | Na | NaOH |
�� | Al2O3 | NaAlO2 | Al | Al(OH)3 | |
�� | FeCl2 | FeCl3 | Fe | CuCl2 | |
�� | Si | SiO2 | Na2SiO3 | H2SiO3 |
A. �٢� B. �ڢ� C. �ڢ� D. �٢�