题目内容
【题目】X、Y、Z、Q、W、R六种短周期元素原子序数依次增大。化合物甲俗称苛性钠,由X、Z、Q三种元素组成。医学中常用QR溶液配制生理盐水。化合物乙由X、R两种元素组成。请回答下列问题:
(1)Q的离子结构示意图为____________________。
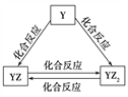
(2)Y元素的单质及其化合物能发生如上图所示的转化,则Y元素为___(填元素符号)。在甲溶液中通入足量YZ2气体,写出该反应的离子方程式:________________________。
(3)W的单质既能与甲溶液反应,又能与乙溶液反应。常温下,将W的单质和甲溶液混合,发生反应的离子方程式为___________________。
【答案】![]() C CO2+OH===HCO3- 2Al+2OH+2H2O===2AlO2-+3H2↑
C CO2+OH===HCO3- 2Al+2OH+2H2O===2AlO2-+3H2↑
【解析】
X、Y、Z、Q、W、R六种短周期元素原子序数依次增大,化合物甲俗称苛性钠,化合物甲由X、Z、Q三种元素组成,则甲为NaOH,X、Z、Q原子序数依次增大,则X是H元素,Z是O元素,Q是Na元素;医学中常用QR溶液配制生理盐水,该化合物是氯化钠,则R是Cl;化合物乙由H、Cl两种元素组成,所以乙为HCl;Y的原子序数小于O元素,根据图示转化关系可知,Y和氧气能生成两种氧化物,根据其化合价可知,Y为C元素;W的单质既能与甲溶液反应,又能与乙溶液反应,则W为Al元素,据此结合元素化合物性质解答。
根据以上分析可知X、Y、Z、Q、W、R六种短周期元素分别是H、C、O、Na、Al、Cl。则
(1)Q是钠,Na+的结构示意图为![]() ;
;
(2)在氢氧化钠溶液中通入足量CO2气体生成碳酸氢钠,该反应的离子方程式为CO2+OH-=HCO3-;
(3)常温下金属铝与氢氧化钠溶液反应生成偏铝酸钠和氢气,发生反应的离子方程式为2Al+2OH-+2H2O=2AlO2-+3H2↑。

【题目】2 L密闭容器中进行反应:pZ(g)+qQ(g) ![]() mX(g)+nY(g),式中m、n、p、q为化学计量数。在0~3 min内,各物质的物质的量的变化如下表所示:
mX(g)+nY(g),式中m、n、p、q为化学计量数。在0~3 min内,各物质的物质的量的变化如下表所示:
物质 | X | Y | Z | Q |
起始/mol | 0.7 | 1 | ||
2 min末/mol | 0.8 | 2.7 | 0.8 | 2.7 |
3 min末/mol | 0.8 |
已知:2 min内v(Q)=0.075 mol·L-1·min-1,v(Z)∶v(Y)=1∶2。
请回答下列问题:
(1)2 min内X的反应速率v(X)=__________。
(2)起始时n(Y)=__________。
(3) 3 min末是否达到平衡_______(填是或否)。
(4)对于该反应,能增大正反应速率的措施是________(填序号,下同)。
A.缩小容器体积 B.移走部分Q
C.通入大量He气 D.升高温度