题目内容
N2(g)+3H2(g) 2NH3(g) △H=-92.4 kJ·mol-1。恒容时,体系中各物质浓度随时间变化的曲线如图示。下列说法错误的是
2NH3(g) △H=-92.4 kJ·mol-1。恒容时,体系中各物质浓度随时间变化的曲线如图示。下列说法错误的是
| A.前20分钟反应内放出的热量为46.2kJ |
| B.第25分钟改变的条件是将NH3从反应体系中分离出去 |
| C.若第60分钟时反应又达到了平衡,则时段Ⅲ改变的条件是降低温度 |
| D.时段Ⅰ仅将初始投放的物质浓度增至原来的2倍,则反应物的转化率增大,平衡常数不变 |
A
解析试题分析:A、不知反应物的物质的量,无法计算反应热,错误;B、第25分钟时只有NH3浓度降低,正确;D、恒容增大初始投放的物质浓度,压强增大,反应物的转化率增大,平衡常数不变,正确。
考点:考查化学平衡有关知识。

练习册系列答案
相关题目
己知反应A(s)+B(g) C(g)+D(g)的化学平衡常数和温度的关系如下:
C(g)+D(g)的化学平衡常数和温度的关系如下:
| 温度(℃) | 700 | 800 | 830 | 1000 | 1200 |
| 化学平衡常数 | 1.7 | 1.1 | 1.0 | 0.6 | 0.4 |
下列说法正确的是
A.该反应的化学平衡常数表达式为:
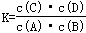
B.该反应为吸热反应
C.单位时间内生成B和D的物质的量相等时,该反应处于平衡状态
D.其它条件不变时,增大体系的压强,化学平衡常数减小
在一定温度下,饱和氯水中存在平衡:Cl2+H2O H++Cl-+HClO。下列说法中确的是
H++Cl-+HClO。下列说法中确的是
A.光照一段时间后,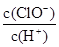 增大 增大 |
| B.加入碳酸钙粉末后,溶液的pH增大 |
| C.加入少量水,由水电离的c(H+)减小 |
| D.加入NaOH固体,一定有c(Na+)>c(Cl-)>c(H+)>c(ClO-)) |
把CoCl2溶解于浓盐酸中,溶液中存在下列平衡:
Co2+ + 4Cl— CoCl4— △H>0
CoCl4— △H>0
粉红色 蓝色
有关上述可逆反应的下列说法不正确的是 ( )
| A.对溶液所在体系加热,溶液蓝色加深 |
| B.对溶液所在体系用冰水降温,上述反应的平衡常数减小 |
| C.室温下,加水稀释,上述反应的平衡常数减小 |
| D.室温下,加水稀释至一定范围,溶液为粉红色 |
在25℃时,密闭容器中X、Y、Z三种气体的初始浓度和平衡浓度如下表:
| 物质 | X | Y | Z |
| 初始浓度/mol·L-1 | 0.1 | 0.2 | 0 |
| 平衡浓度/mol·L-1 | 0.05 | 0.05 | 0.1 |
下列说法错误的是
A.反应达到平衡时,X的转化率为50%
B.反应可表示为X+3Y
 2Z,其平衡常数值为1600
2Z,其平衡常数值为1600C.增大压强使平衡向生成Z的方向移动,平衡常数增大
D.改变温度可以改变此反应的平衡常数
向甲、乙、丙三个密闭容器中充人一定量的A和B,发生反应:xA(g)+B(g) 2C(g)。各容器的反应温度、反应物起始量,反应过程中C的浓度随时间变化关系分别以下表和下图表示 ( )
| 容器 | 甲 | 乙 | 丙 |
| 容积 | 0.5L | 0.5L | 1. 0L |
| 温度/ | T1 | T2 | T3 |
| 反应物 起始量 | 0.5molA 1.5 molB | 0.5 molA 1.5 molB | 2.0 molA 6.0 molB |
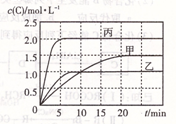
下列说法正确的是
A.由图可知:T1<T2,且该反应为吸热反应
B.T2时该反应的平衡常数K=0.8
C.l0min内甲容器中反应的平均速率v(B)=0.025mol·(L·min)-1
D.T1℃,若起始时甲容器中充入1.5molA、0.5molB,平衡时B的转化率为25%
一定温度下,在甲、乙、丙、丁四个恒容密闭容器中投入SO2(g)和O2(g),其起始物质的量及SO2的平衡转化率如下表所示。
| | 甲 | 乙 | 丙 | 丁 | |
| 密闭容器体积/L | 2 | 2 | 2 | 1 | |
| 起始物质的量 | n(SO2)/mol | 0.4 | 0.8 | 0.8 | 0.4 |
| n(O2)/mol | 0.24 | 0.24 | 0.48 | 0.24 | |
| SO2的平衡转化率/% | 80 | α1 | α2 | α3 | |
下列判断中,正确的是
A.甲中反应的平衡常数小于乙
B.该温度下,甲和乙中反应的平衡常数K均为400
C.SO2的平衡转化率:α1>α2=α3
D.容器中SO3的物质的量浓度:丙>甲=丁
对化学反应限度的叙述,错误的是
| A.任何可逆反应都有一定的限度 |
| B.化学反应达到限度时,正逆反应速率相等 |
| C.化学反应的限度与时间的长短无关 |
| D.化学反应的限度是不可改变的 |
