��Ŀ����
��ס��ҡ��������ܱ������г���һ������A��B��������Ӧ��xA(g)+B(g) 2C(g)���������ķ�Ӧ�¶ȡ���Ӧ����ʼ������Ӧ������C��Ũ����ʱ��仯��ϵ�ֱ����±�����ͼ��ʾ �� ��
| ���� | �� | �� | �� |
| �ݻ� | 0.5L | 0.5L | 1. 0L |
| �¶ȣ� | T1 | T2 | T3 |
| ��Ӧ�� ��ʼ�� | 0.5molA 1.5 molB | 0.5 molA 1.5 molB | 2.0 molA 6.0 molB |
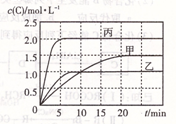
����˵����ȷ����
A����ͼ��֪��T1<T2���Ҹ÷�ӦΪ���ȷ�Ӧ
B��T2ʱ�÷�Ӧ��ƽ�ⳣ��K=0.8
C��l0min�ڼ������з�Ӧ��ƽ������v(B)=0.025mol��(L��min)��1
D��T1�棬����ʼʱ�������г���1.5molA��0.5molB��ƽ��ʱB��ת����Ϊ25%
B
�������������A����ͼ��֪���ҷ�Ӧ���ʿ죬�¶ȸߣ�T1<T2������C��Ũ�ȵͣ��¶ȸ߷�Ӧ������У���ӦΪ���ȷ�Ӧ������B��������֪�ҡ���Ϊ��Чƽ�⣨���ɷ����������ͬ����������ѹǿ��ͬ������ֻ���Ƿ�Ӧ��ѧ��Ӧ����ʽ��������������ȣ���x=1������ɵ�K=0.8����ȷ��C��l0min�ڼ������з�Ӧ��ƽ������v(C)=0.1mol��(L��min)��1����v(B)=0.05mol��(L��min)��1������D��T1�棬����ʼʱ�������г���1.5molA��0.5molB�������0.5molA��1.5molB�ǵ�Ч�ģ�A��B��������ͬ��������ƽ��ʱC������Ϊ0.75mol����Ӧ��n(B)= n(C)��2=0.375mol������B��ת����Ϊ0.375��0.5=75%������
���㣺���黯ѧƽ����ƽ����ƶ���ƽ�ⳣ����ת���ʡ���Ӧ���ʵ��йؼ�������ݡ�

��һ���¶��£�������ijһ��Ӧ��M��N������������ʵ����淴Ӧʱ��仯��������ͼ�����б�������ȷ��( )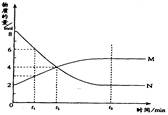
A����Ӧ�Ļ�ѧ����ʽΪ��2M N N |
| B��t2ʱ�����淴Ӧ������ȣ��ﵽƽ�� |
| C��t3ʱ������Ӧ���ʴ����淴Ӧ���� |
| D��t1ʱ��N��Ũ����MŨ�ȵ�2�� |
T Kʱ����2.0 L�����ܱ������г���1.0 mol COCl2����ӦCOCl2(g) Cl2(g)��CO(g)������һ��ʱ���ﵽƽ�⡣��Ӧ�����вⶨ�IJ������ݼ��±���
Cl2(g)��CO(g)������һ��ʱ���ﵽƽ�⡣��Ӧ�����вⶨ�IJ������ݼ��±���
| t / s | 0 | 2 | 4 | 6 | 8 |
| n(Cl2) / mol | 0 | 0.16 | 0.19 | 0. 20 | 0.20 |
����˵����ȷ����
A����Ӧ��ǰ2 s ��ƽ������v(CO)= 0.080mol��L��1��s��1
B�����������������䣬�����¶ȣ�ƽ��ʱc(Cl2)=" 0.11" mol��L��1����Ӧ�Ħ�H��0
C��T Kʱ��ʼ�������г���0.9 mol COCl2��0.10 mol Cl2��0.10 mol CO����Ӧ�ﵽƽ��ǰv��>v��
D��T Kʱ��ʼ�������г���1.0 mol Cl2��0.9 mol CO���ﵽƽ��ʱ��Cl2��ת����С��80%
N2(g)+3H2(g) 2NH3(g) ��H����92.4 kJ��mol-1������ʱ����ϵ�и�����Ũ����ʱ��仯��������ͼʾ������˵���������
2NH3(g) ��H����92.4 kJ��mol-1������ʱ����ϵ�и�����Ũ����ʱ��仯��������ͼʾ������˵���������
| A��ǰ20���ӷ�Ӧ�ڷų�������Ϊ46.2kJ |
| B����25���Ӹı�������ǽ�NH3�ӷ�Ӧ��ϵ�з����ȥ |
| C������60����ʱ��Ӧ�ִﵽ��ƽ�⣬��ʱ��ı�������ǽ����¶� |
| D��ʱ�������ʼͶ�ŵ�����Ũ������ԭ����2������Ӧ���ת��������ƽ�ⳣ������ |
ij�¶������ݻ�������ܱ������У�����aX��g��+bY��g�� cW��g����Ӧ��������1 mol X��lmol Y���ﵽƽ��ʱ��W��Ũ��Ϊ0��2 mol/L������˵���������
cW��g����Ӧ��������1 mol X��lmol Y���ﵽƽ��ʱ��W��Ũ��Ϊ0��2 mol/L������˵���������
| A���ﵽƽ��ʱ������b mol Y��ͬʱ����c moI W |
| B���������¶ȣ�W�����ʵ���Ũ�ȼ�С����÷�Ӧ��H<0 |
| C������ʼͶ��X��Y�����ʵ����ֱ�Ϊamol��bmol����ƽ��ʱX��Y��ת������� |
| D������ͬ�����£��ٳ���l mol X��1 mol Y������ƽ��ʱ��W��Ũ��Ϊ0��4 mol/L����a+b>c |
��һ�������£��̶��ݻ����ܱ������з�Ӧ��2NO2(g) 2NO (g) +O2 (g) ��H��0���ﵽƽ�⡣���ı�����һ������X��Y��X�ı仯����ͼ�����ߵ���
2NO (g) +O2 (g) ��H��0���ﵽƽ�⡣���ı�����һ������X��Y��X�ı仯����ͼ�����ߵ���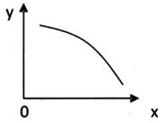
| A����X��ʾ�¶�ʱ��Y��ʾNO2�����ʵ��� |
| B����X��ʾѹǿʱ��Y��ʾNO2��ת���� |
| C����X��ʾ��Ӧʱ��ʱ��Y��ʾ���������ܶ� |
| D����X��ʾNO2�����ʵ���ʱ��Y��ʾO2�����ʵ��� |
��һ���¶��£���������˵�����淴ӦA��g��+2B(g)
 2C(g) �ﵽƽ��ģ� ��
2C(g) �ﵽƽ��ģ� ��
A��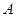 �� ��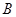 �� ��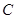 ��Ũ��֮��Ϊ1:2:2 ��Ũ��֮��Ϊ1:2:2 |
B����λʱ��������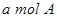 ��ͬʱ����2a mol C ��ͬʱ����2a mol C |
C��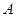 ��Ũ�Ȳ��ٱ仯 ��Ũ�Ȳ��ٱ仯 |
| D��������������ʵ���Ϊ2a mol |
 2Z(g) ��H��
2Z(g) ��H�� ����ͼ�Ƿ�Ӧ��ƽ�⼰�ı�����ƽ���ƶ���ͼ������˵���������
����ͼ�Ƿ�Ӧ��ƽ�⼰�ı�����ƽ���ƶ���ͼ������˵���������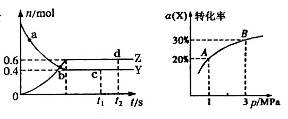
 zC(g)��ͼI��ʾ200��ʱ������A��B��C���ʵ�����ʱ��ı仯��ͼ���ʾ��ͬ�¶���ƽ��ʱC�������������ʼn(A):n(B)�ı仯��ϵ�������н�����ȷ����
zC(g)��ͼI��ʾ200��ʱ������A��B��C���ʵ�����ʱ��ı仯��ͼ���ʾ��ͬ�¶���ƽ��ʱC�������������ʼn(A):n(B)�ı仯��ϵ�������н�����ȷ����