题目内容
6.6g碳和8g氧气高温下在一密闭容器中充分反应,若碳和氧气均反应完全,则所得气体产物是( )| A. | 14g CO2 | B. | 1lg CO2、3g CO | C. | CO、CO2各7g | D. | 14g CO |
分析 6gC完全反应生成CO需要氧气质量=$\frac{\frac{6g}{12g/mol}}{2}$×32g/mol=8g,所以C和氧气恰好完全反应生成CO,再结合质量守恒来分析解答.
解答 解:6gC完全反应生成CO需要氧气质量=$\frac{\frac{6g}{12g/mol}}{2}$×32g/mol=8g,所以C和氧气恰好完全反应生成CO,根据质量守恒定律知,生成一氧化碳质量=6g+8g=14g,故选D.
点评 本题考查化学方程式有关计算,为高频考点,正确判断C和氧气反应产物是解本题关键,再结合质量守恒定律来分析解答.

练习册系列答案
 轻松课堂单元期中期末专题冲刺100分系列答案
轻松课堂单元期中期末专题冲刺100分系列答案
相关题目
16.元素的原子核外有四个电子层,其3d能级上的电子数是4s能级上的3倍,则此元素是( )
| A. | S | B. | Fe | C. | Si | D. | Cl |
14.已知一定条件下,黄铁矿与硫酸铁溶液反应的化学方程式为FeS2+7Fe2(SO4)3+8H2O═15FeSO4+8H2SO4,下列说法错误的是( )
| A. | FeS2是还原剂,发生氧化反应 | |
| B. | FeSO4是还原产物 | |
| C. | 每生成1molH2SO4,转移14mol电子 | |
| D. | 反应中H2O既不是氧化剂也不是还原剂 |
1.下列变化属于化学变化的是( )
| A. | 空气液化制取氮气 | B. | 蒸馏法将海水淡化为饮用水 | ||
| C. | 过滤、蒸发将粗盐提纯 | D. | 酸雨侵蚀建筑物 |
11.下列表示对应化学反应的离子方程式正确的是( )
| A. | 向稀HNO3 中滴加Na2SO3溶液:SO32-+2H+═SO2↑+H2O | |
| B. | 向Na2SiO3溶液中通入过量CO2:SiO32-+2CO2+H2O═H2SiO3↓+2HCO3- | |
| C. | 向Al2(SO4)3 溶液中加入过量NH3•H2O:Al3++4NH3.H2O═AlO2-+4NH4++2H2O | |
| D. | NaHCO3溶液中加少量Ba(OH)2溶液:2HCO3-+Ba2++2OH-═BaCO3↓+2H2O+CO32- |
18.下列各组物质中,X是主体物质,Y是少量杂质,Z是为除去杂质所要加入的试剂,其中所加试剂正确的一组是( )
| A | B | C | D | |
| X | FeCl2溶液 | FeCl2溶液 | Fe | FeSO4溶液 |
| Y | FeCl3 | CuCl2 | Al | Fe2(SO4)3 |
| Z | Cl2 | Fe | NaOH溶液 | Cu |
| A. | A | B. | B | C. | C | D. | D |
15.在火星上工作的美国“勇气号”、“机遇号”探测车的一个重要任务就是收集有关Fe2O3及硫酸盐的信息,以证明火星上存在或曾经存在过水,以下叙述正确的是( )
| A. | Fe2O3是一种酸性氧化物 | |
| B. | 检验从火星上带回来的红色物质是否是Fe2O3的操作步骤为:样品-→粉碎-→加水溶解-→过滤-→向滤液中滴加KSCN溶液 | |
| C. | 分别还原a mol Fe2O3所需H2、Al、CO的物质的量之比为 3:2:3 | |
| D. | 明矾属硫酸盐,含结晶水,是混合物 |
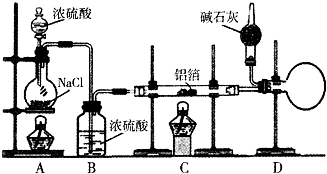 无水氯化铝是有机化工常用的催化剂,氯化铝178℃时升华,极易潮解,遇水发热并产生白色烟雾.氯化铝还易溶于乙醇、氯仿和四氯化碳.实验室可用反应2Al+6HCl(g)$\frac{\underline{\;\;△\;\;}}{\;}$2AlCl3+3H2制备少量无水氯化铝,某同学利用该原理设计如下实验装置:
无水氯化铝是有机化工常用的催化剂,氯化铝178℃时升华,极易潮解,遇水发热并产生白色烟雾.氯化铝还易溶于乙醇、氯仿和四氯化碳.实验室可用反应2Al+6HCl(g)$\frac{\underline{\;\;△\;\;}}{\;}$2AlCl3+3H2制备少量无水氯化铝,某同学利用该原理设计如下实验装置: