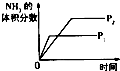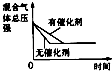题目内容
【题目】用 A 质子数 B 中子数 C 核外电子数 D 最外层电子数 E 电子层数 填写下列空白:
(1)原子种类由_______决定;
(2)元素种类由_______决定;
(3)元素的化学性质主要由_______决定;
(4)元素的原子半径由_______决定;
(5)元素的化合价主要由_______决定。
【答案】AB A D AE D
【解析】
(1)原子种类由质子数和中子数决定,故选AB;
(2)元素是指质子数相同一类原子或离子的统称,由质子数决定,故选A;
(3)元素的化学性质主要由最外层电子决定,故选D;
(4)元素的原子半径由质子数和电子层数决定,故选AE;
(5)元素的化合价主要由最外层电子决定,故选D;

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
【题目】已知如表25℃时某些弱酸的电离平衡常数.如图表示常温时,稀释CH3COOH、HClO两种酸的稀溶液时,溶液pH随加水量的变化.依据所给信息,下列说法正确的是( )
CH3COOH | HClO | H2CO3 |
Ka=1.8×10﹣5 | Ka=3.0×10﹣8 | Ka1=4.4×10﹣7 Ka2=4.7×10﹣11 |

A.如图中的两种酸分别和等浓度的NaOH溶液刚好完全反应,消耗碱的体积相等
B.向NaClO溶液中通入少量二氧化碳的离子方程式为:2ClO﹣+CO2+H2O═2HClO+CO32﹣
C.a、b、c三点所示溶液中水的电离程度c>a>b
D.图象中,Ⅰ表示CH3COOH,Ⅱ表示HClO,且溶液导电性:c>b>a
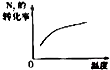
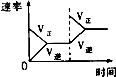
【题目】对于可逆反应N2(g)+3H2(g)2NH3(g)△H<0,下列研究目的和示意图相符的是( )
A | B | C | D | |
研究目的 | 压强对反应的影响(P2>P1) | 温度对反应的影响 | 平衡体系增加N2对反应的影响 | 催化剂对反应的影响 |
图示 |
|
|
|
|
A.A
B.B
C.C
D.D